eQMS: Automatización de la calidad
Qué es un sistema de gestión de la calidad (SGC)
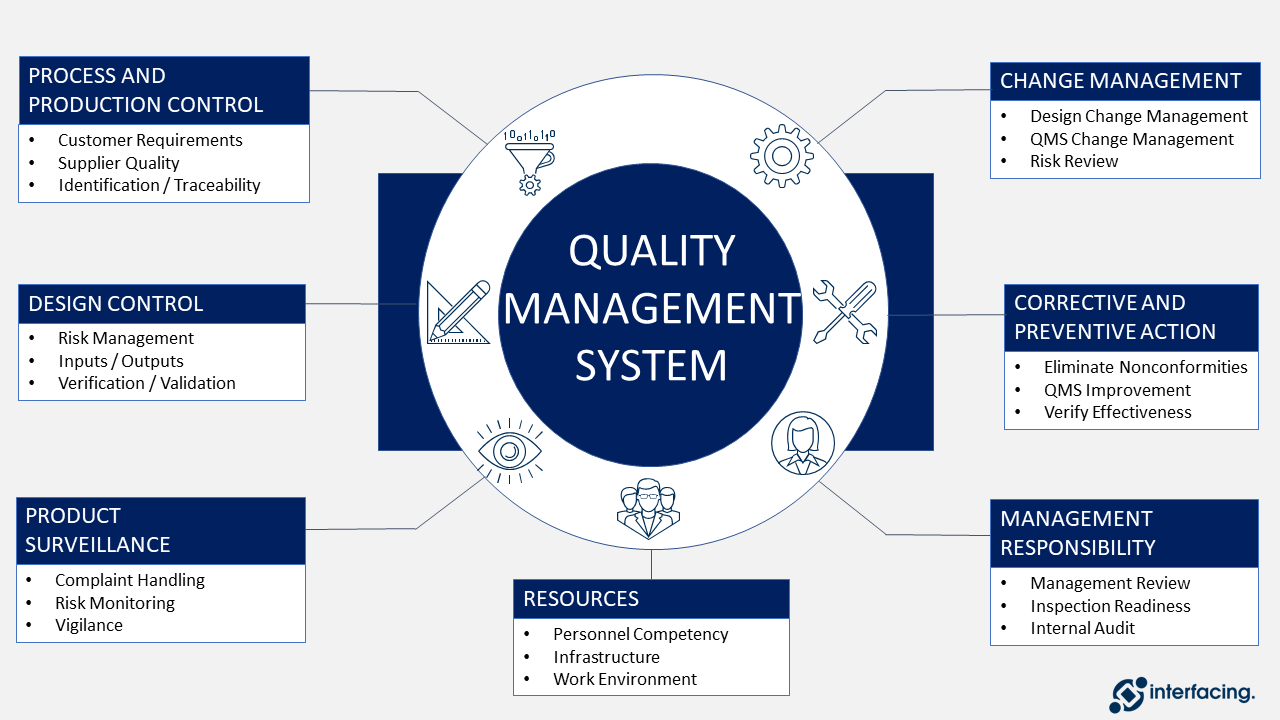
Según la ASQ (American Society of Quality): el sistema de gestión de la calidad (SGC) se define como un sistema formalizado que documenta los procesos, procedimientos y responsabilidades para alcanzar las políticas y objetivos de calidad. Un SGC ayuda a coordinar y dirigir las actividades de una organización para cumplir con los requisitos reglamentarios y del cliente y mejorar su eficacia y eficiencia de forma continua.
Consulte la imagen siguiente para ver un desglose del diseño básico del SGC como estructura general.
Sistema electrónico de gestión de la calidad (EQMS)
Hoy en día, las organizaciones están obligadas a garantizar la calidad, el cumplimiento y muchas otras normas específicas del sector en relación con sus procesos de producción y prestación de servicios. Para garantizar que estas normativas cumplen con los estándares de la industria, las empresas adoptarán una solución de sistema de gestión de calidad eQMS.
Estas soluciones de eQMS han cambiado progresivamente con el tiempo, habiendo comenzado como hojas de cálculo básicas en un principio. Las empresas aprovecharían estas hojas de cálculo para el seguimiento y la gestión de sus procesos de calidad. Con la evolución de los recursos informáticos, los sistemas eQMS surgieron como soluciones de software fiables que ejecutan procesos, identifican responsabilidades y detallan procedimientos para la consecución de objetivos y el cumplimiento de políticas. Piense en ello como una plataforma QMS que está integrada con una infraestructura de TI y un modelo de datos que facilita la comunicación y la colaboración interfuncional.
Si bien existen capacidades personalizadas variables integradas según la industria, las plataformas de entrega, el tamaño de la organización, etc., hay algunas capacidades típicas en las que comúnmente se invierte. Estos incluirían:
- Plataforma basada en web
- Adoptar un enfoque de BPM para la funcionalidad implica aplicaciones que se construyen en una plataforma con integración con otras aplicaciones.
- Interoperabilidad con otras aplicaciones de planificación de recursos empresariales (ERP).
- La interfaz grafica se basa en roles y se centra en la ejecución del proceso de flujo de trabajo.
Capacidades de eQMS de Interfacing
Gestión de documentos y registros
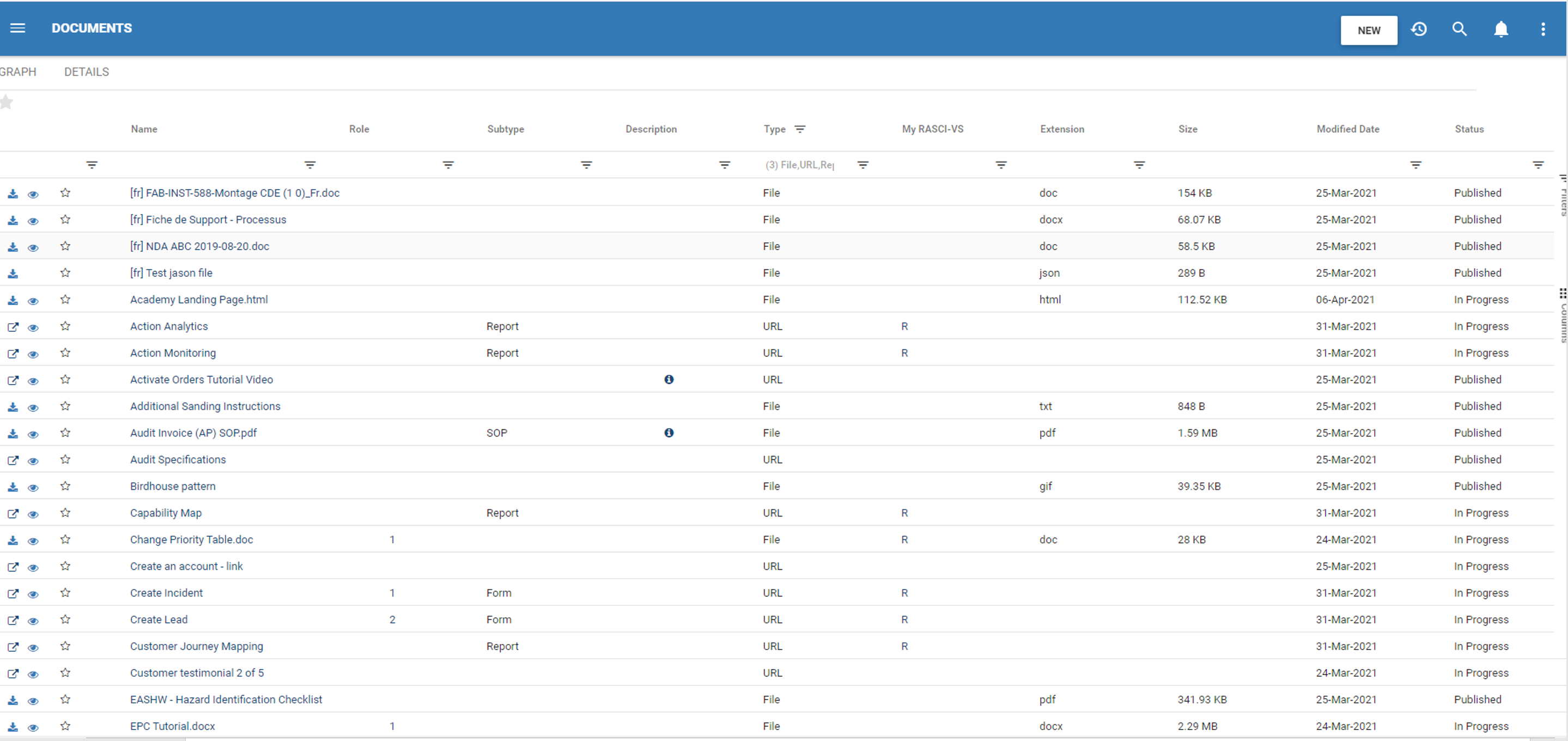
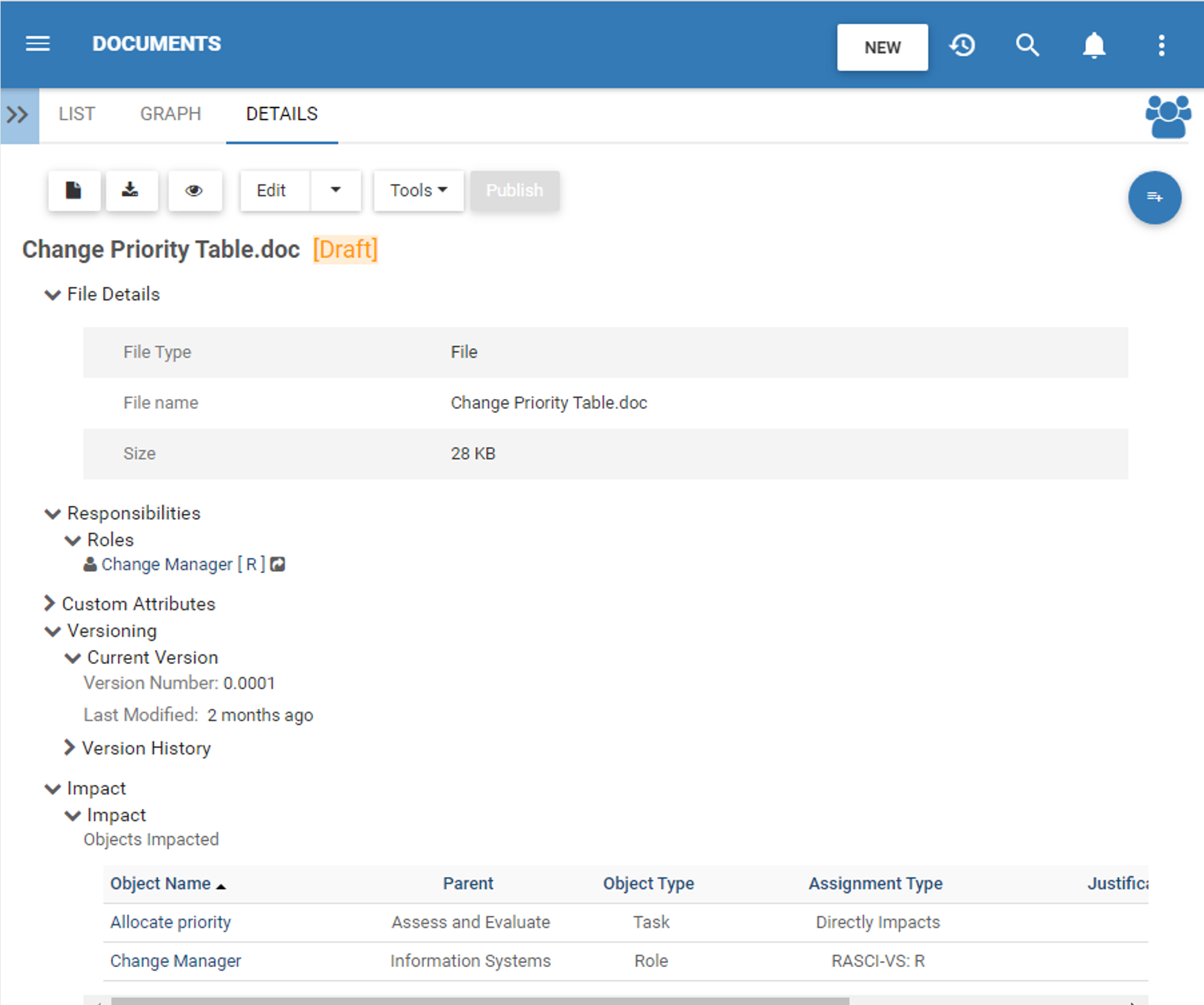
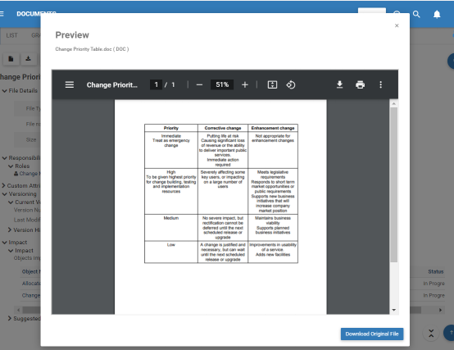
En la actualidad, mantener un sistema de documentos en papel que cumpla la norma ISO es todo un reto, si no casi imposible. El conjunto de características de los sistemas sería engorroso, propenso a los errores y a la pérdida de tiempo. Su productividad aumentaría significativamente al automatizar todas las tareas repetitivas asociadas a la gestión de documentos del SGC. El eQMS de EPC añade una clara visibilidad al ciclo de vida de los documentos y supervisará de forma proactiva el estado del flujo de trabajo de su organización, al tiempo que mejora la eficiencia del sistema de calidad.
Los equipos dispersos geográficamente pueden ahora conectarse, colaborar, ser coautores, corregir, revisar, comentar y firmar documentos, todo ello de forma electrónica y segura dentro del sistema. Las notificaciones automáticas por correo electrónico y los acuses de recibo ayudan a los sistemas a agilizar el proceso de distribución en toda la organización La retención automática de documentos, la impresión, las revisiones periódicas y el archivado son totalmente conformes y se controlan mediante la codificación USFDA 21 CFR parte 11, lo que hace que las auditorías y las inspecciones de calidad estén libres de preocupaciones.
Características principales:
- Añadir nuevos documentos
- Identificaciones y etiquetas únicas por documento
- Control de versiones por documento
- Archivar, mover y eliminar documentos existentes
- Estructurar el documento en una jerarquía, carpetas
- Crea plantillas para los registros y la capacidad de reutilizar la plantilla de flujo de trabajo
- Registro de auditoría / rastro de los cambios en los metadatos
- Flujo de trabajo para aprobaciones y revisiones
- Firma electrónica de las aprobaciones
- Delegación en las revisiones y aprobaciones
- Notificaciones, correos electrónicos para los flujos de trabajo
- Comprobación del sistema de publicaciones y aprobaciones
- Colaborar y plantear solicitudes de cambio
- Soporte multilingüe: interfaz de usuario, sugerencias de traducción de metadatos y documentos
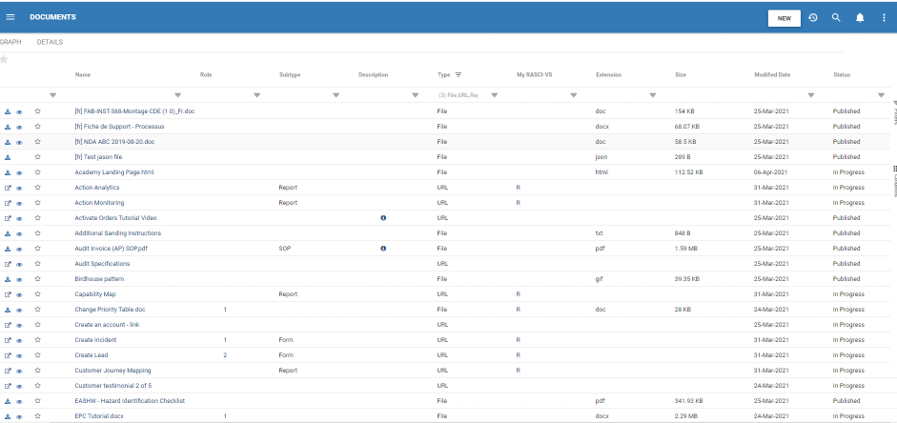
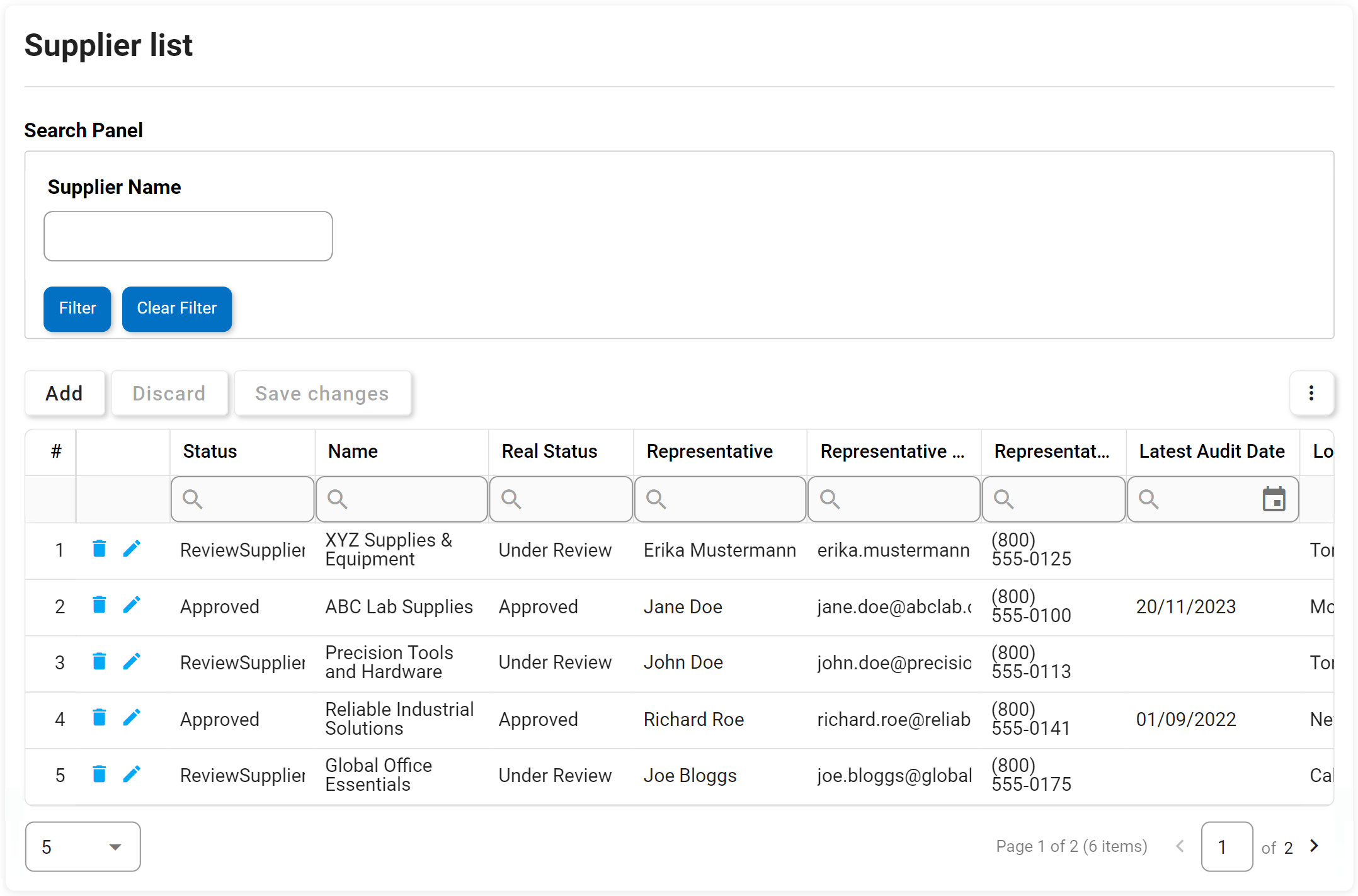
Potente búsqueda de documentos por:
- Nombre del documento
- Identificación del documento
- Unidad organizacional
- Texto completo
- Metadatos (Tipo, Categorías, Atributos)
- Columnas filtrables
- Últimos datos modificados
- Modificado por última vez por
- Cualquier atributo definido por el usuario (UDA)
Gestión de auditorías
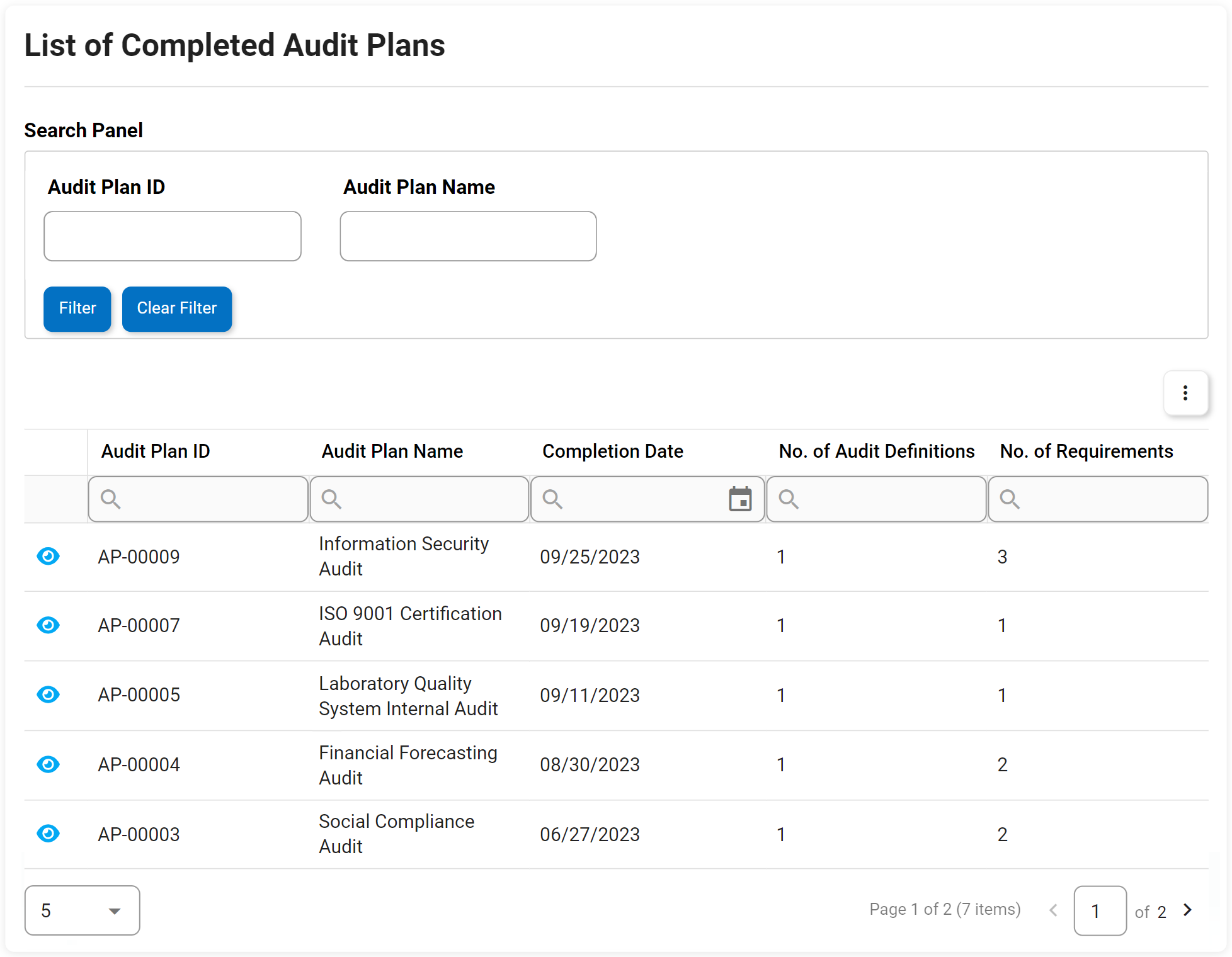
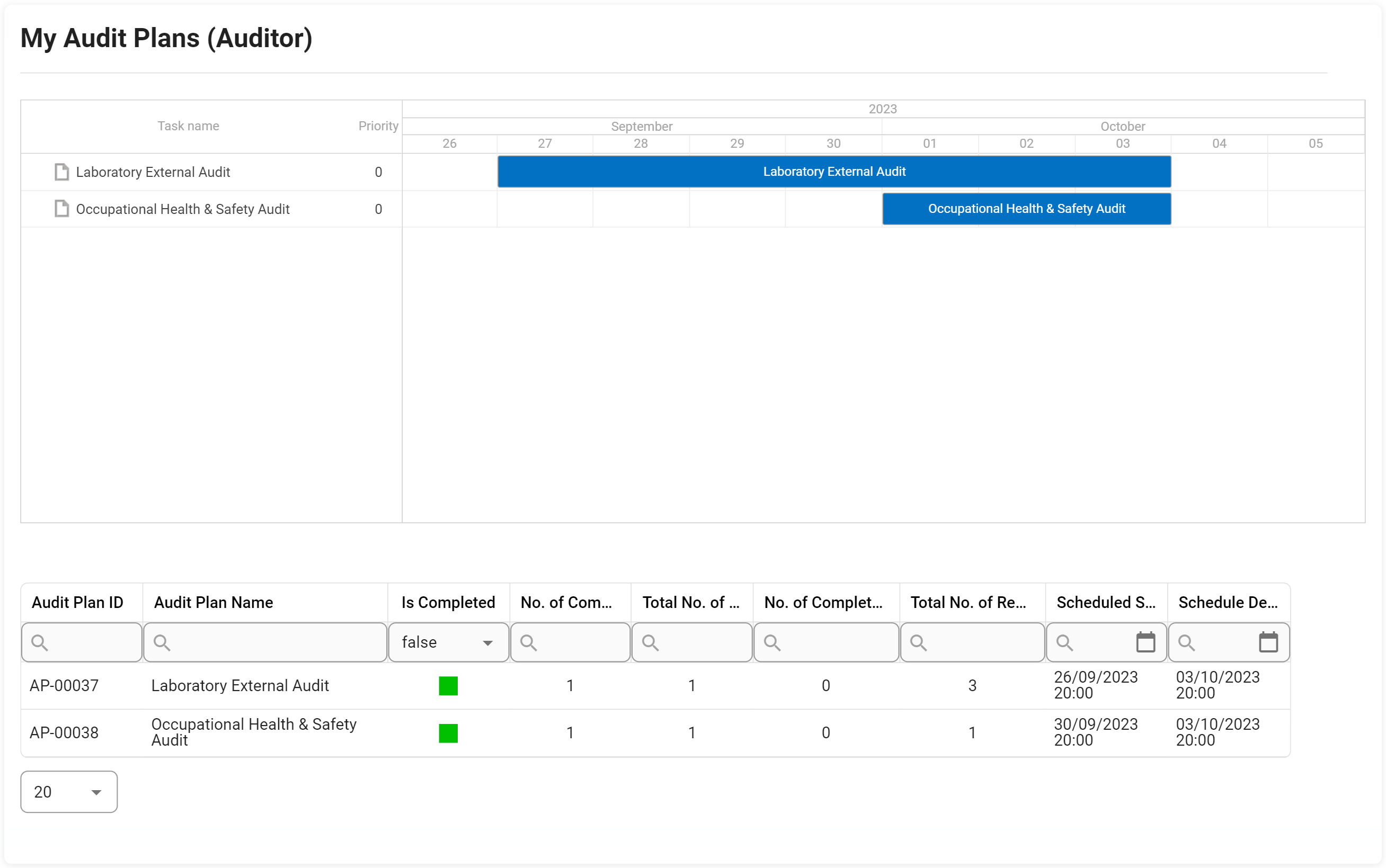
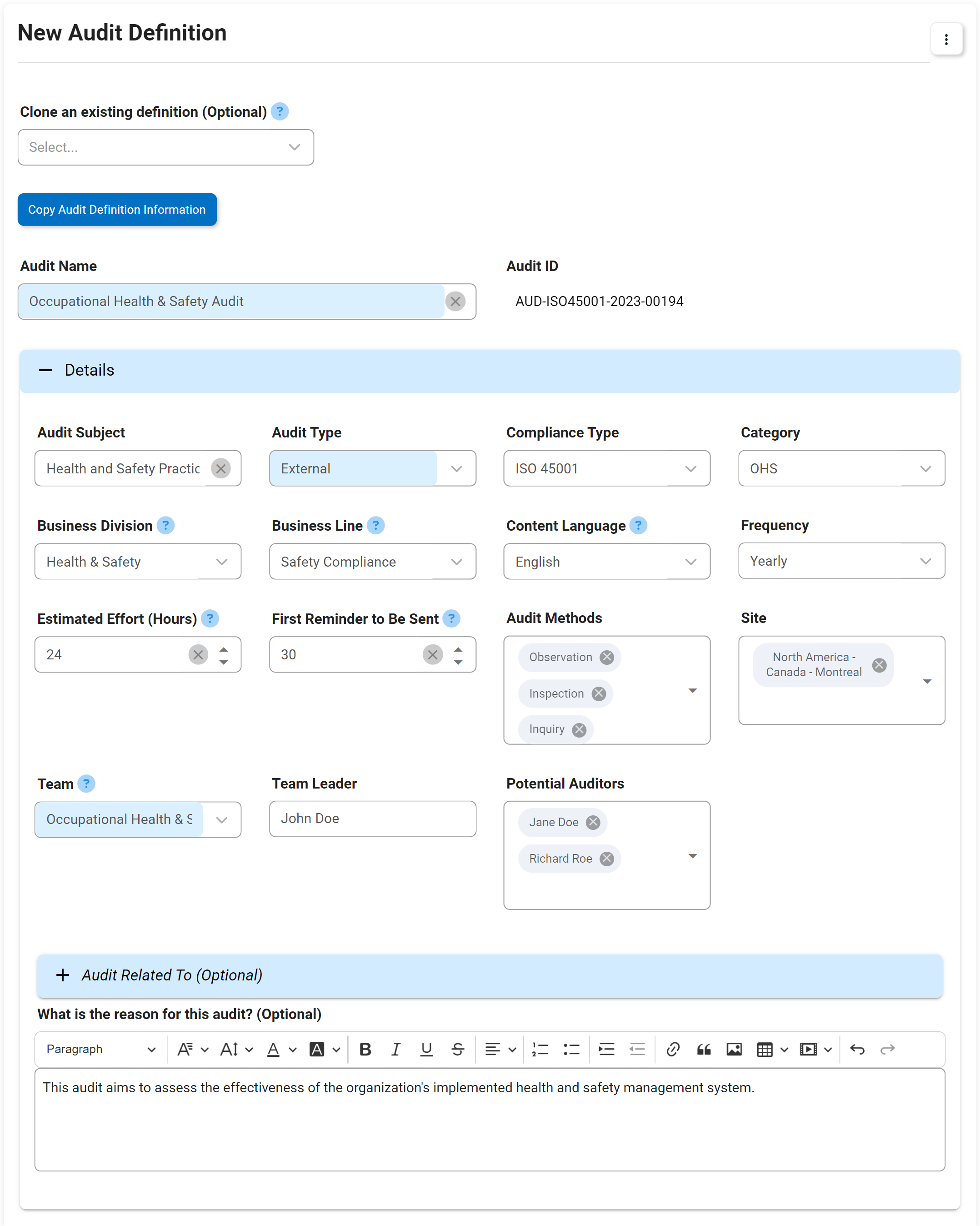
El apoyo a la gestión de auditorías de Interfacing para su organización incluye el cumplimiento de las normas de una amplia variedad de auditorías internas y externas. Las normas de la FDA, la ISO, la calidad y las auditorías clínicas son algunos de los organismos que establecen las especificaciones de conformidad que deben cumplirse. Nuestro DBP automatizará las tareas que normalmente se realizan de forma manual en Excel, ofreciendo la posibilidad de reutilizar las definiciones de auditoría y los requisitos de pruebas, evidencias y muestreo; lo que significa que sólo tendrá que definir los requisitos de auditoría y pruebas una vez, y utilizarlos en múltiples auditorías. Esto incluye la capacidad de realizar auditorías tanto internas como externas (proveedores, clientes, requisitos reglamentarios, etc.).
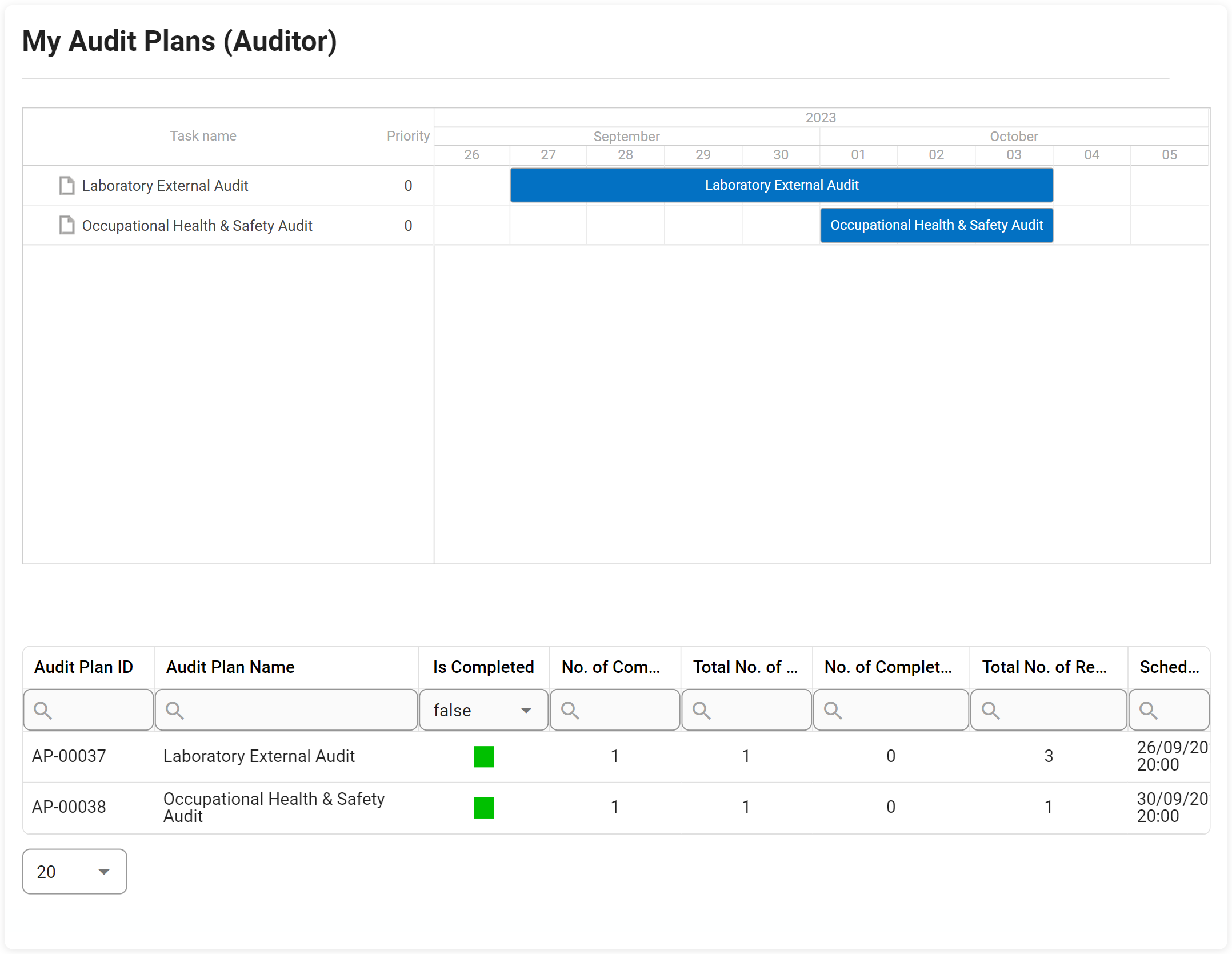
Al utilizar nuestra plataforma empresarial digital, no sólo podrá seguir la auditoría paso a paso, sino que también podrá escalar la auditoría con hallazgos mayores/menores hasta el CAPA en la gestión de elementos de acción. Una de nuestras herramientas se utiliza en las charlas de Gantt sobre la planificación de auditorías, la gestión de la capacidad, la gestión de los requisitos ISO, etc.
Características principales:
- Captura de todas las instancias de auditoría y pruebas en un solo repositorio
- Busque y ordene los campos de auditoría por ID, nombre, frecuencia, tamaño de la muestra, etc.
- Auditoría ad hoc iniciada y auditoría programada
- Establezca los atributos clave de la auditoría, como el auditor y el auditado, la fecha límite, el activador para iniciar, el requisito previo, etc.
- Ver, editar y añadir resultados de muestras para diferentes fines de auditoría
- Determinar la eficacia y la precisión de las muestras mediante botones de automatización
- Ensayos e informes de auditoría completos
Activadores, escalamiento y validación
- Activar el CAPA a través de auditorías fallidas, incidentes o solicitudes ad hoc
- Añadir múltiples elementos de acción (AI) que definan criterios específicos (por ejemplo, nombre de AI, propietario, tipo de acción, prioridad, etc.)
- Asignar IAs a recursos específicos con plazos claros y nivel de prioridad
- Escalamiento automático de la solicitud de CAPA a su propietario de IA o a un rol diferente de igual responsabilidad en caso de ausencia de su propietario de IA
- Permitir que el propietario de la IA solicite una prórroga para su IA asignada
- Recoger y almacenar las pruebas de IA para validar su realización
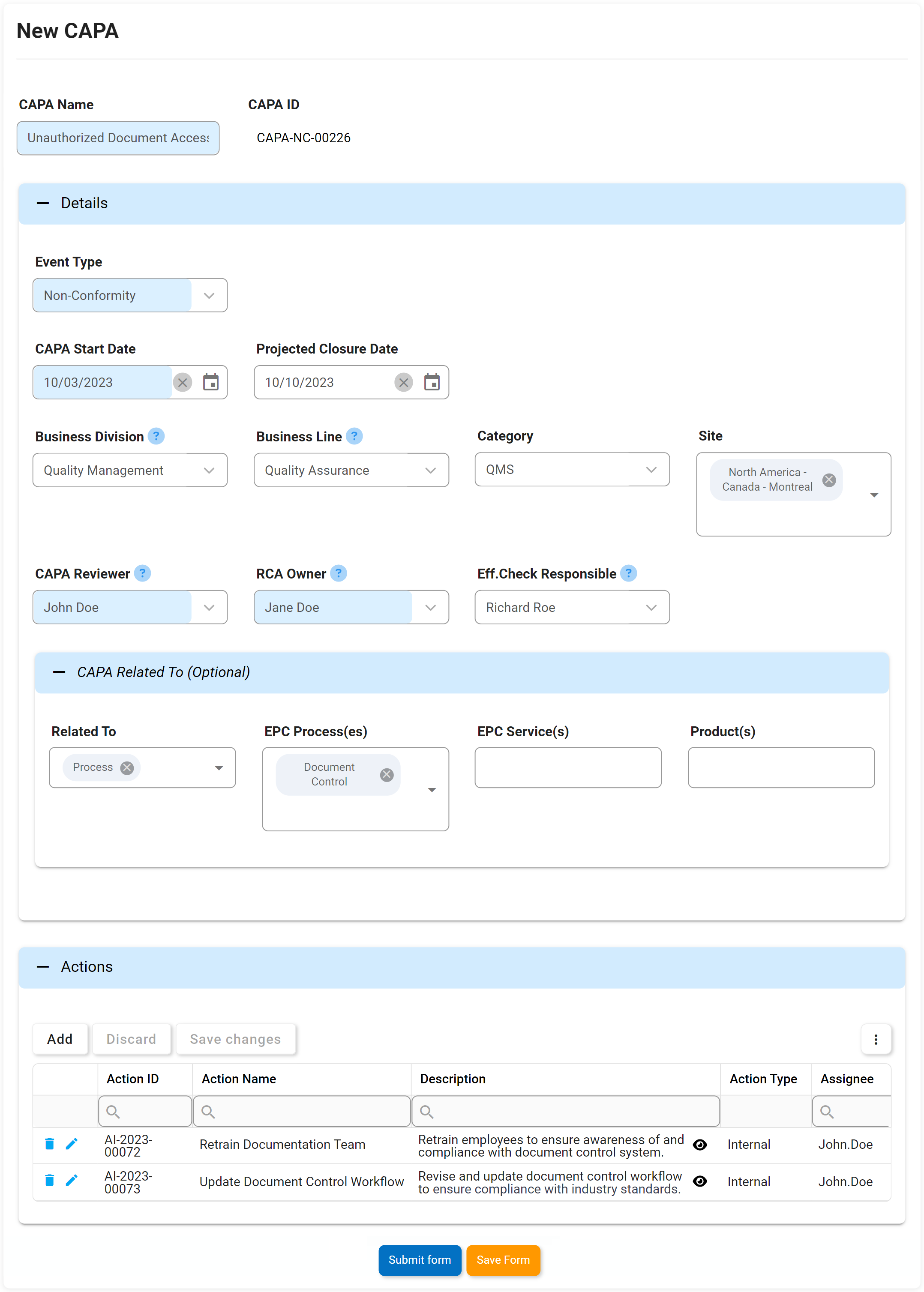
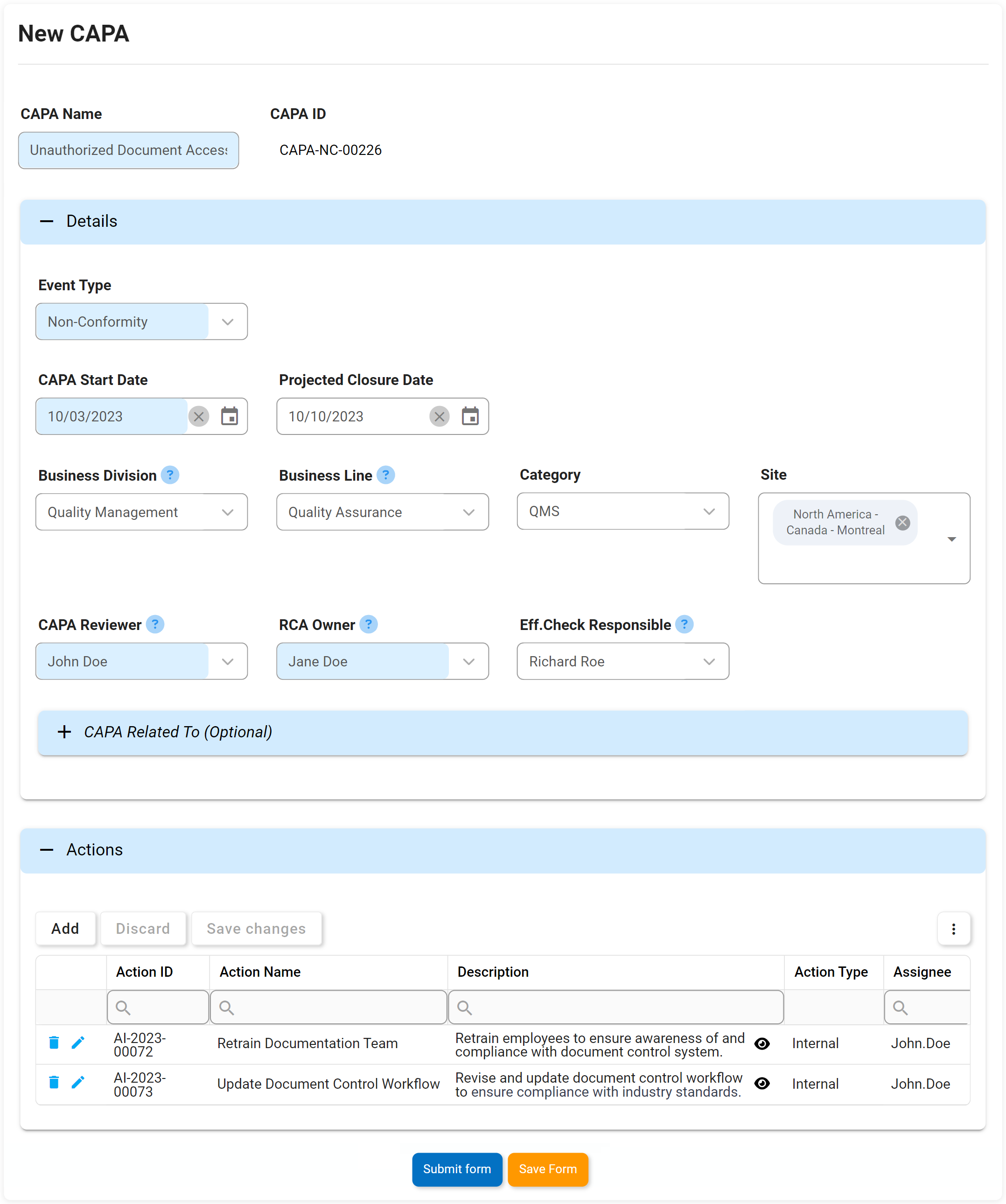
Acciones Correctivas y Preventivas (CAPA)
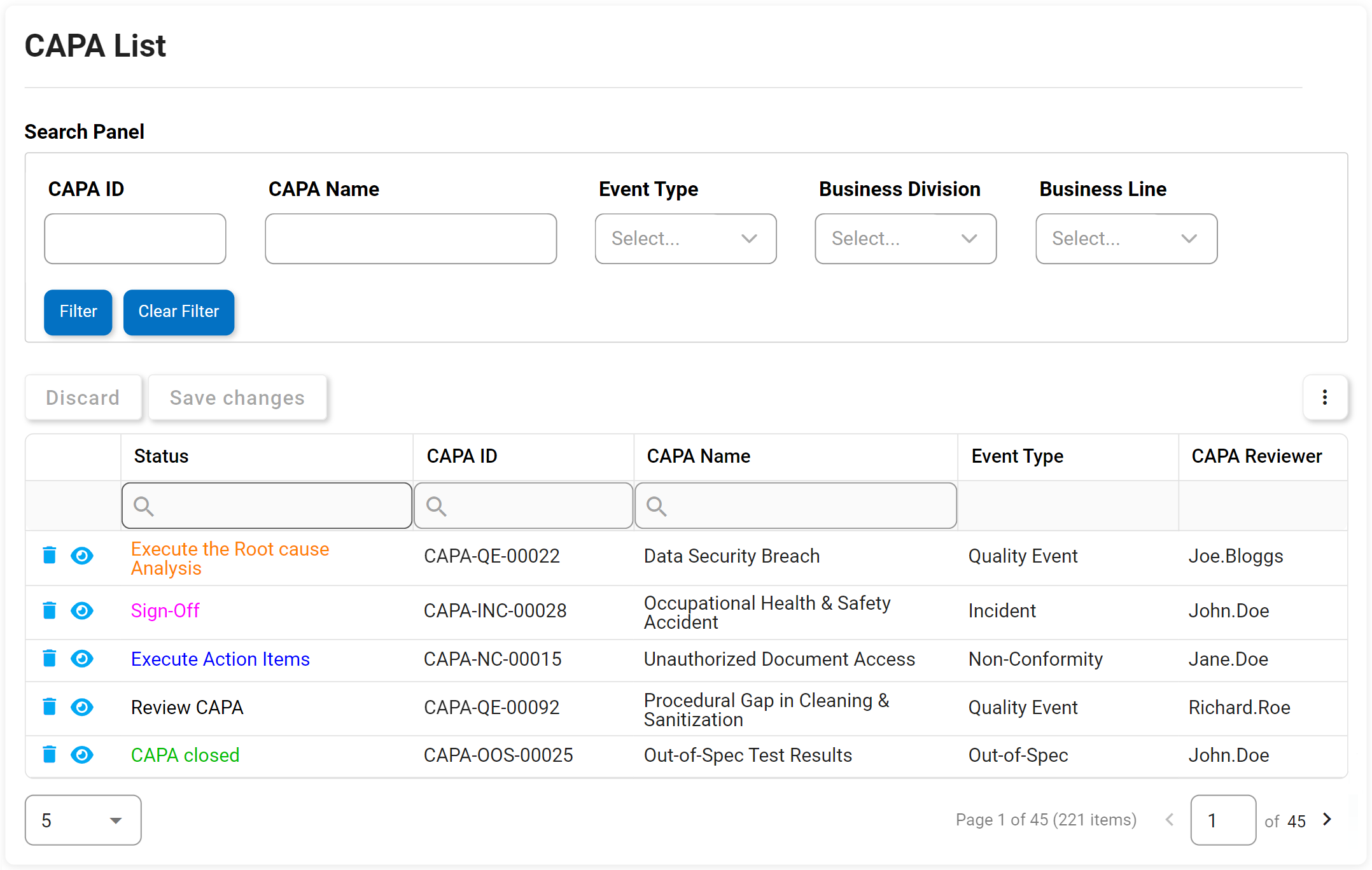
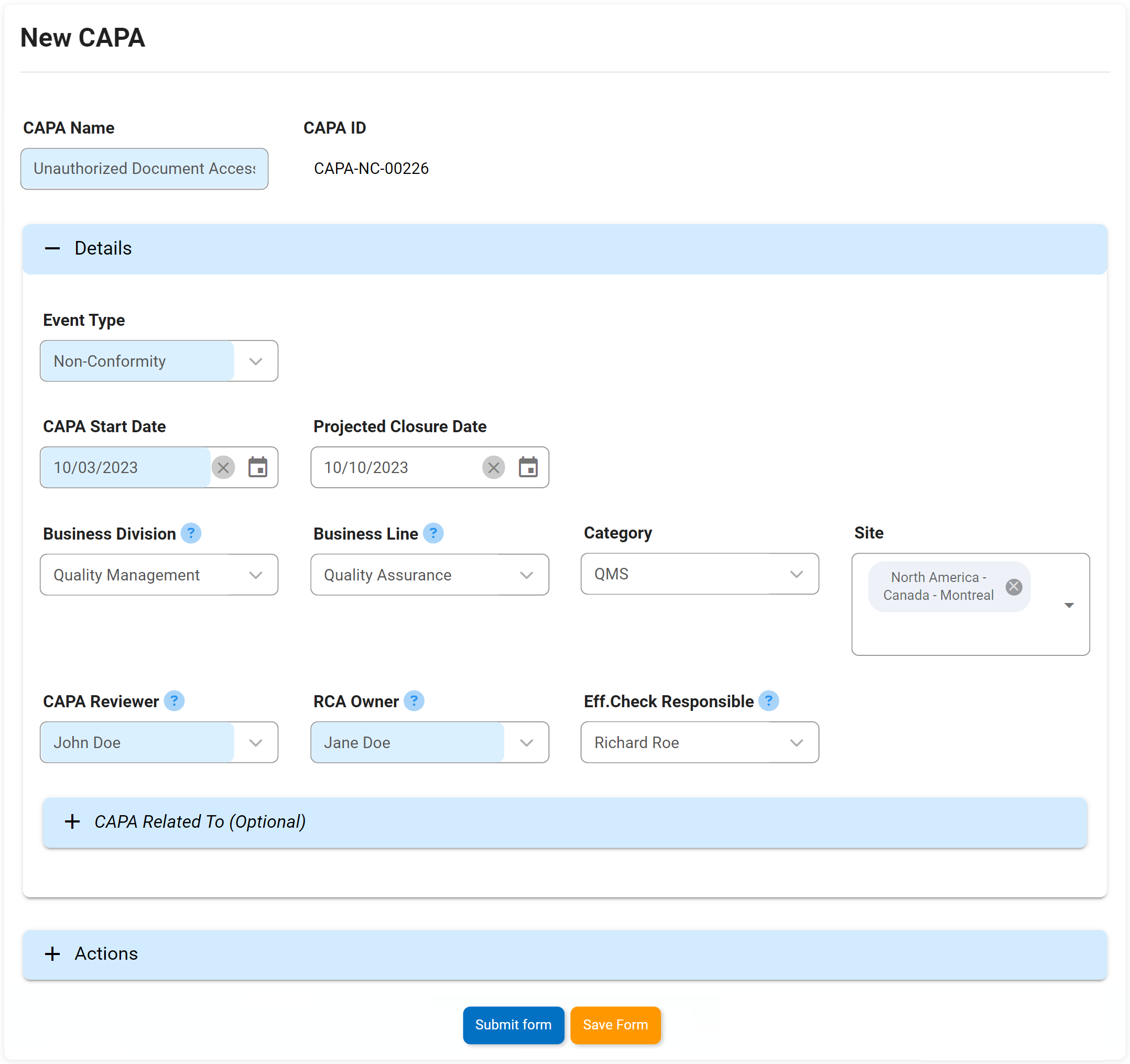
Pensamos en el CAPA como en el sistema inmunológico de una organización. Si se produce una desviación o un fallo sistémico en los procesos o pasos de fabricación de una organización, el CAPA es el proceso riguroso que identificará por qué se ha producido el defecto o el fallo. La Acción Correctiva Preventiva (CAPA) es el proceso utilizado para investigar y resolver los problemas de las organizaciones, e identificará y tomará medidas correctivas para evitar que vuelvan a producirse las causas fundamentales. El DBP (Digital Business Platform) de Interfacing ayuda a CAPA a prevenir la reaparición de cualquier causa raíz de un fallo o defecto.
Nuestro DBP (Dgital Business Platform) se planteará de forma ad hoc o como resultado de los resultados de una investigación de incidentes o auditorías. Planteará acciones que puedan rastrearse hasta una fuente y aplicarse como parte de un plan de gestión de elementos de acción.
Atributos clave:
- Fecha de la subida
- Tipo
- Fecha límite
- Descripción del problema
- Causa principal
- Elementos de acción CAPA
- Pestaña de información de la prueba: muestra todas las pruebas completadas heredadas del formulario anterior
- Información sobre auditorías o incidentes fallidos heredados del formulario
- Ver/editar/añadir múltiples elementos de acción CAPA
- Funciones responsables y estado de los elementos de acción disponibles en tiempo real
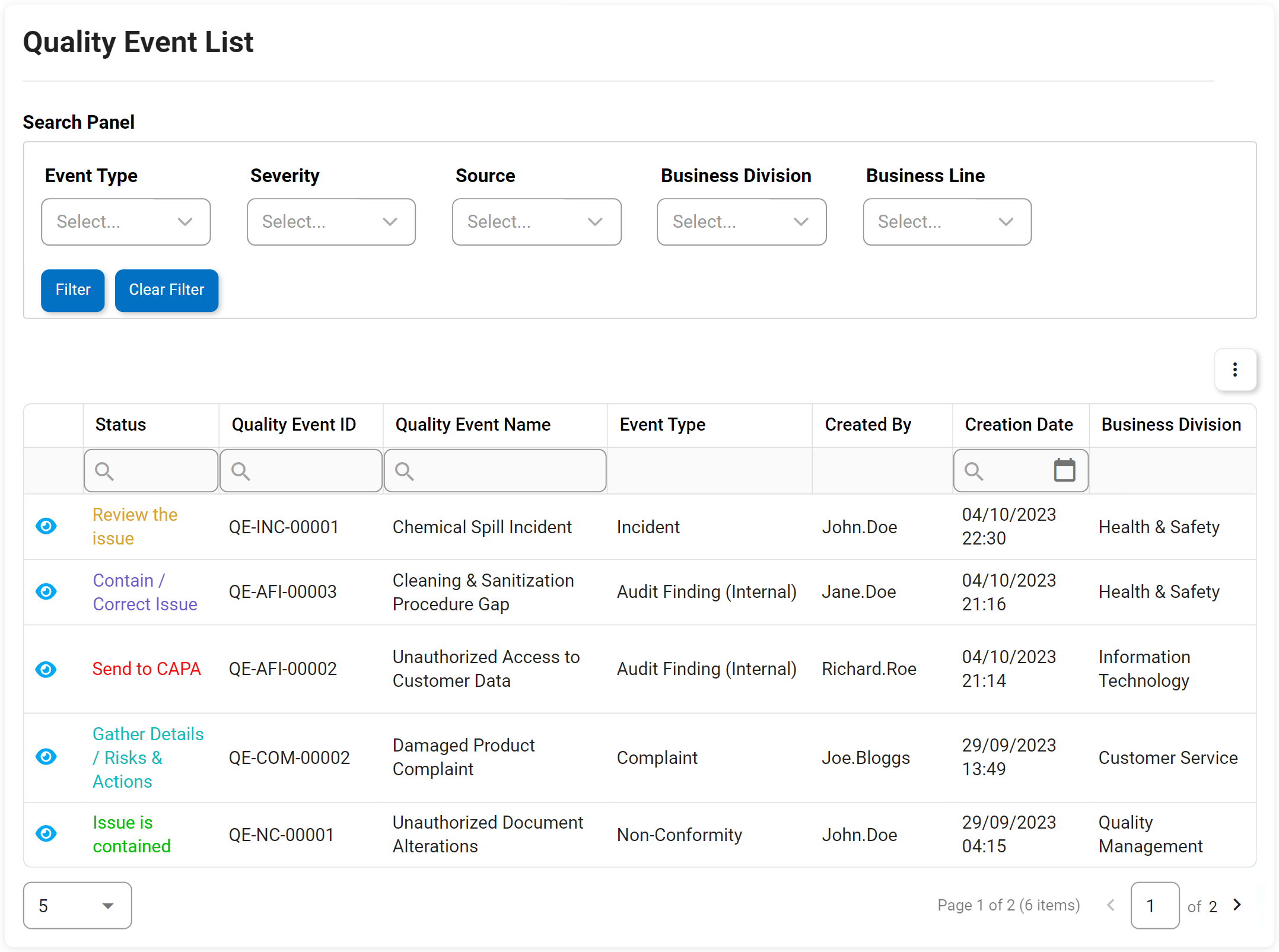
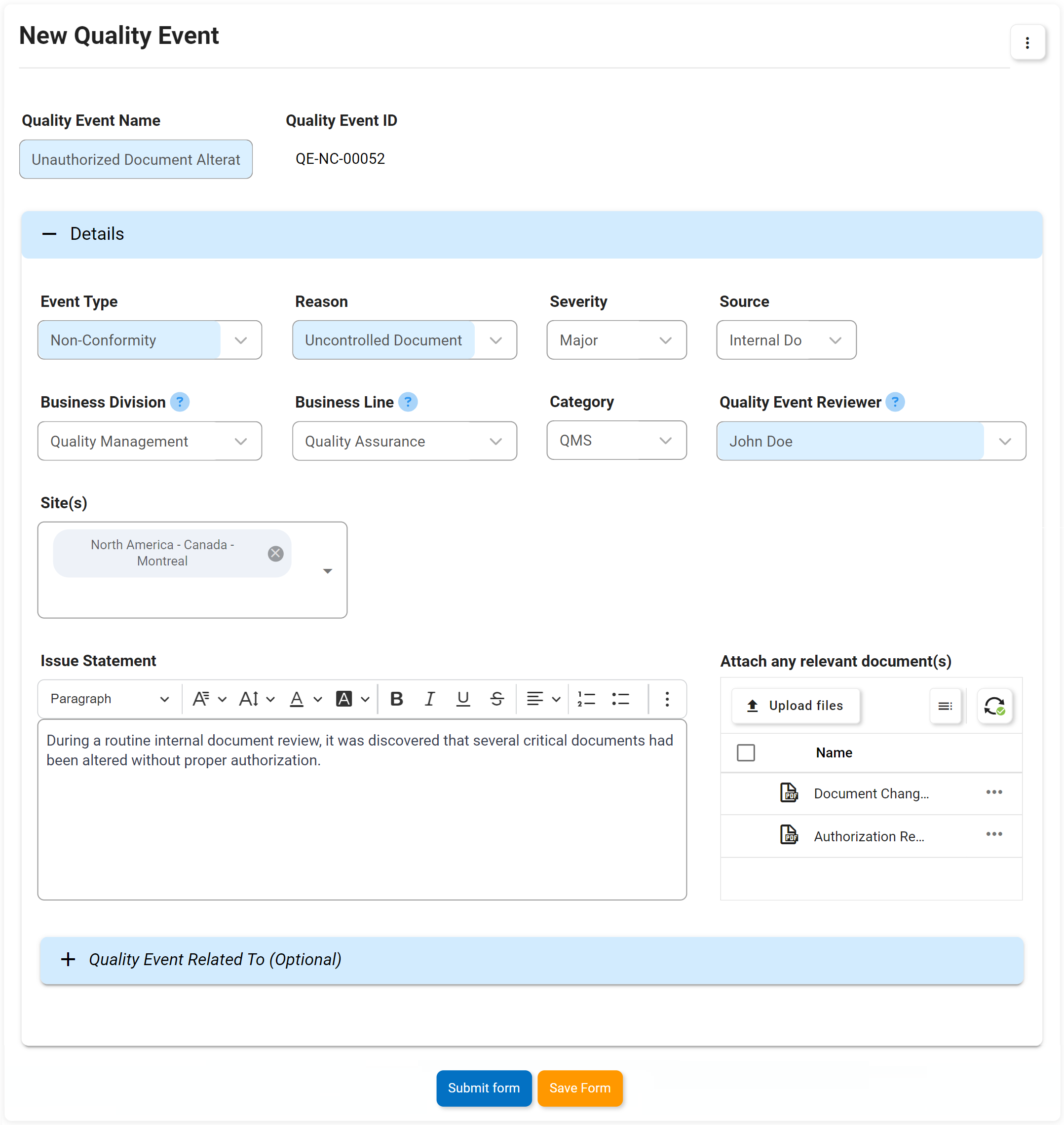
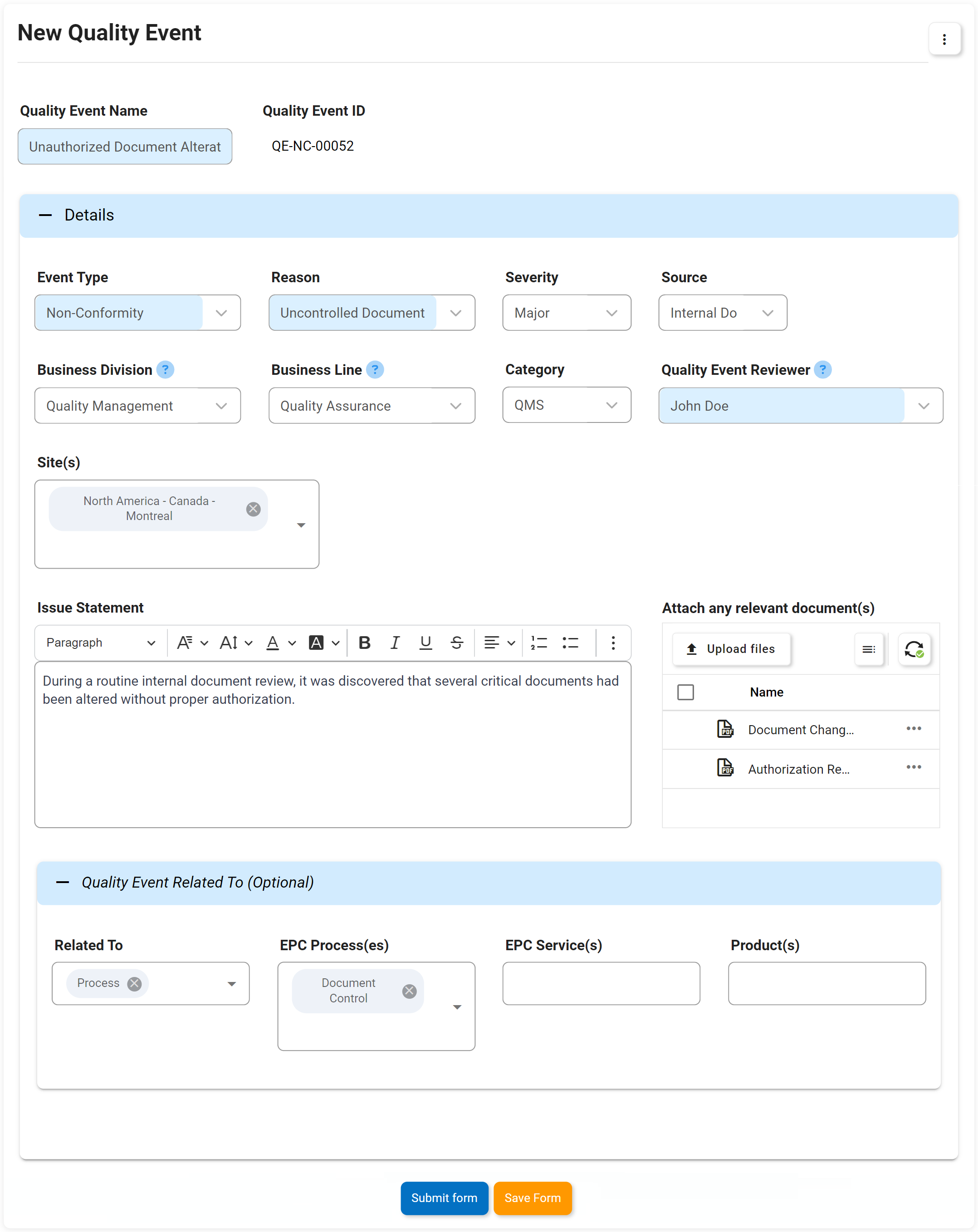
Eventos de Calidad incluyendo No Conformidad, Quejas, etc.
La gestión de las no conformidades es un requisito para cumplir las normas ISO 9001. La solución de software eQMS Digital Business Platform (DBP) de Interfacing combina la gestión de documentos y procesos para mejorar significativamente la gestión de cualquier no conformidad y sus planes de acción asociados. Con nuestro DBP, puede identificar y plantear los problemas de no conformidad descubiertos en una auditoría para crear un plan de gestión de elementos de acción. Los beneficios son impactantes. En otro ejemplo, en un proceso de producción, las anomalías pueden identificarse en la fase de diseño, lo que ahorra un gasto importante respecto a las que se resuelven más adelante en el proceso de fabricación o incluso en la distribución o en la venta al consumidor.
La aplicación y el seguimiento de las no conformidades y la eficacia de cada una de ellas para evitar operaciones empresariales adversas son posibles gracias al eQMS. Con un eQMS, cada incidente se registrará con todos los elementos de acción asociados.
Características principales:
- Identificación de la causa raíz, motivo principal de la NC o de lo que ha fallado
- Por qué el trabajo no cumple las especificaciones
- Qué se puede hacer para evitar que el problema se repita
- Explicación de las medidas correctoras adoptadas o por adoptar
- Personas clave implicadas en la NC y especificaciones afectadas por la NC
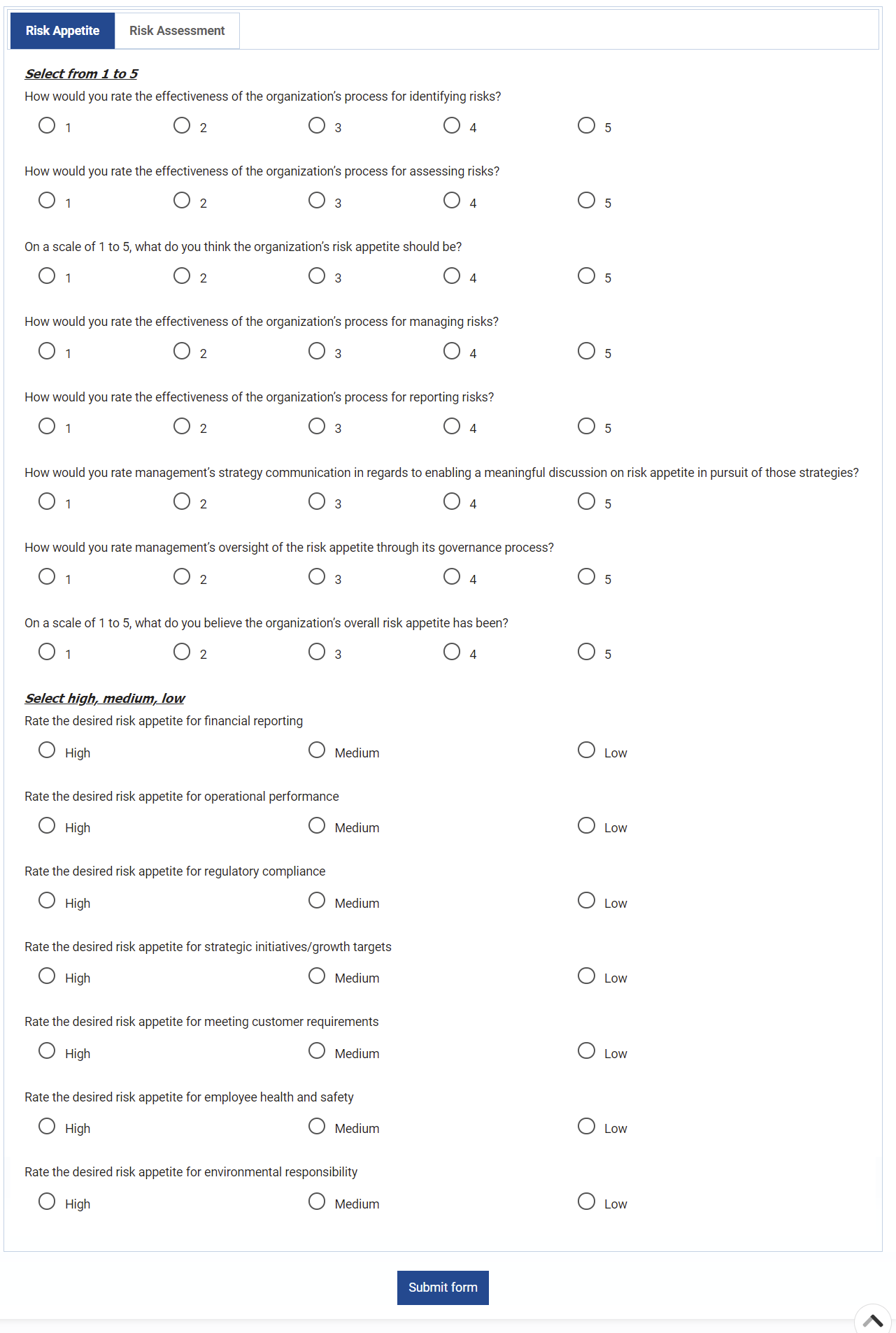
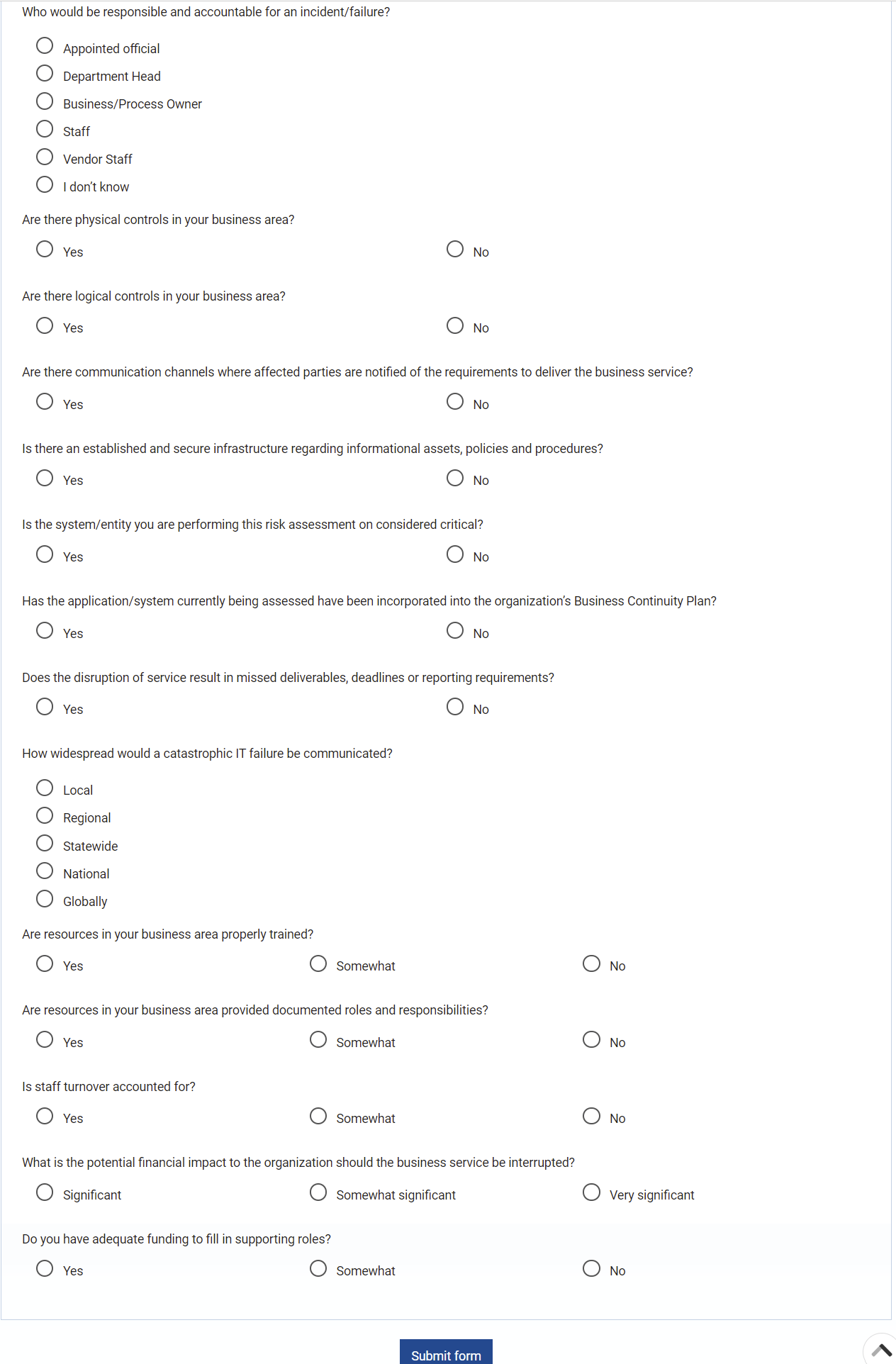
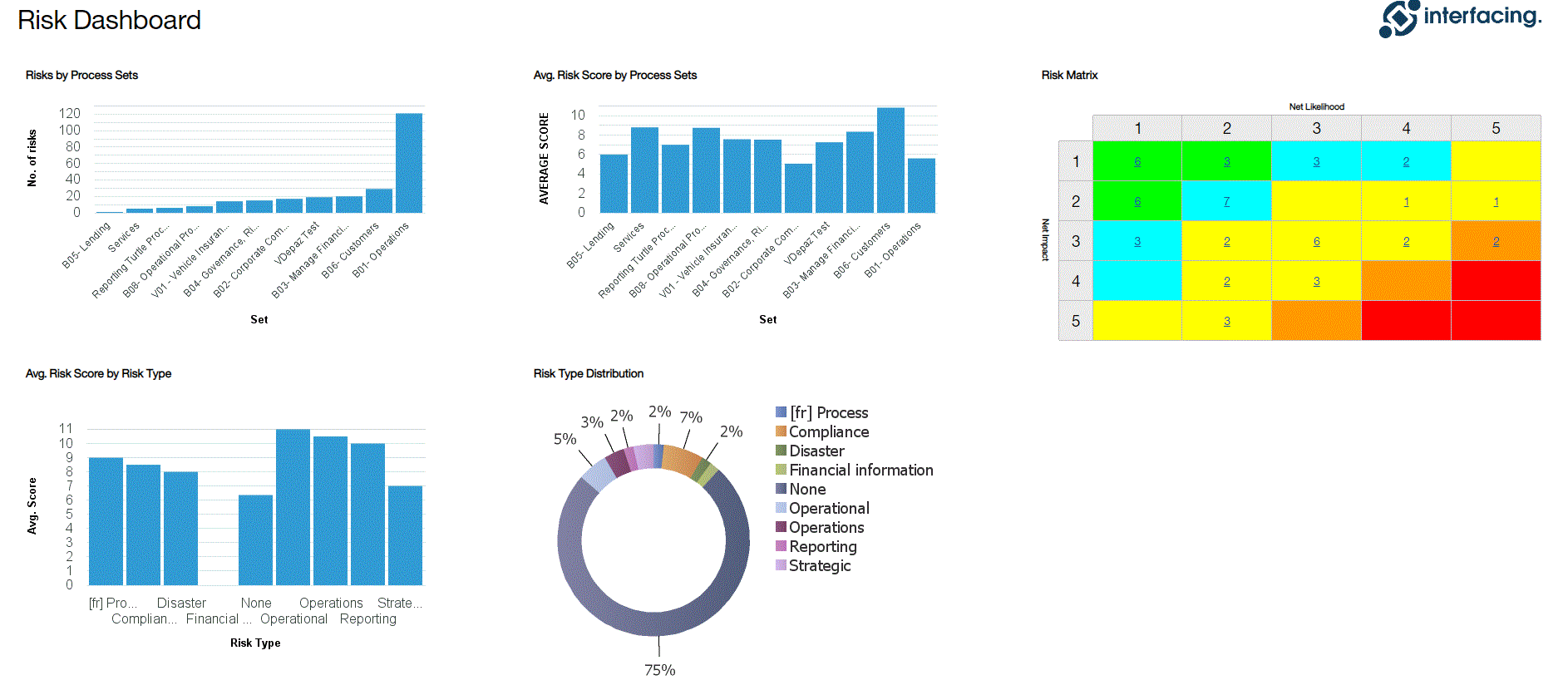
Gestión de Riesgos
Enterprise Process Center® (EPC) facilita que las organizaciones sean proactivas frente a reactivas cuando se trata de estrategias de control de riesgos y gestión de riesgos de procesos. La gestión de riesgos no solo es importante para protegerse contra desastres, sino que al integrar controles en las operaciones diarias puede garantizar que se cumplan los estándares de calidad y se mantenga la satisfacción del cliente. Además, no hay nada más grande que el coste del “incumplimiento”, por lo que la transparencia integral de los riesgos y los procesos es una necesidad para cumplir con las leyes y los requisitos reglamentarios como Sarbanes Oxley, Basilea III, FMI, HIPAA, FDA, ISO 15000, entre otros.
Características principales:
- Biblioteca de riesgos detallada que incluye el identificador, la descripción, el tipo, la categoría y los recursos responsables (a través de RASCI-VS)
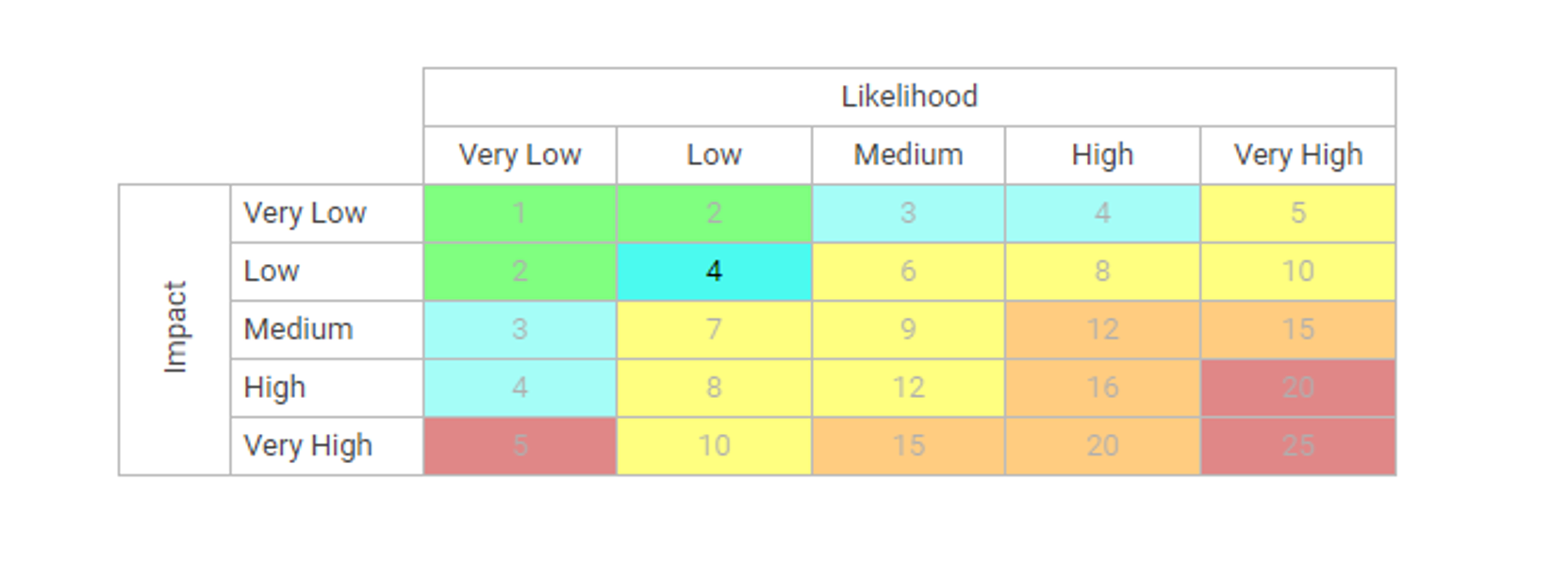
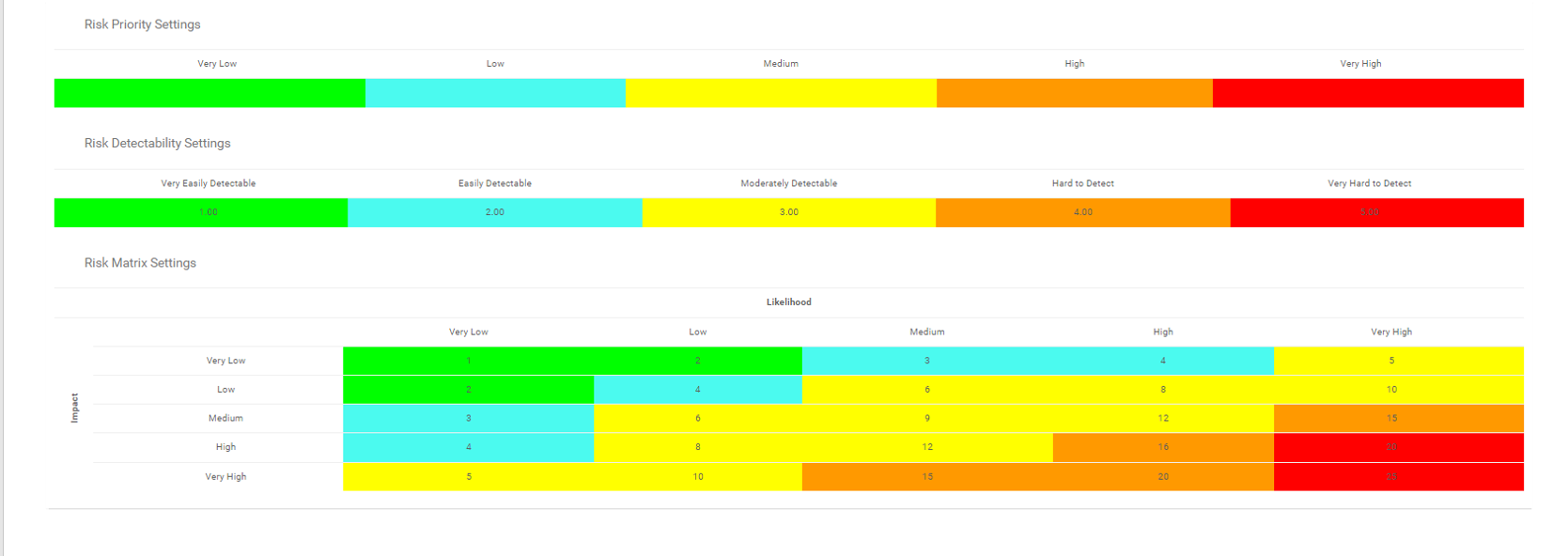
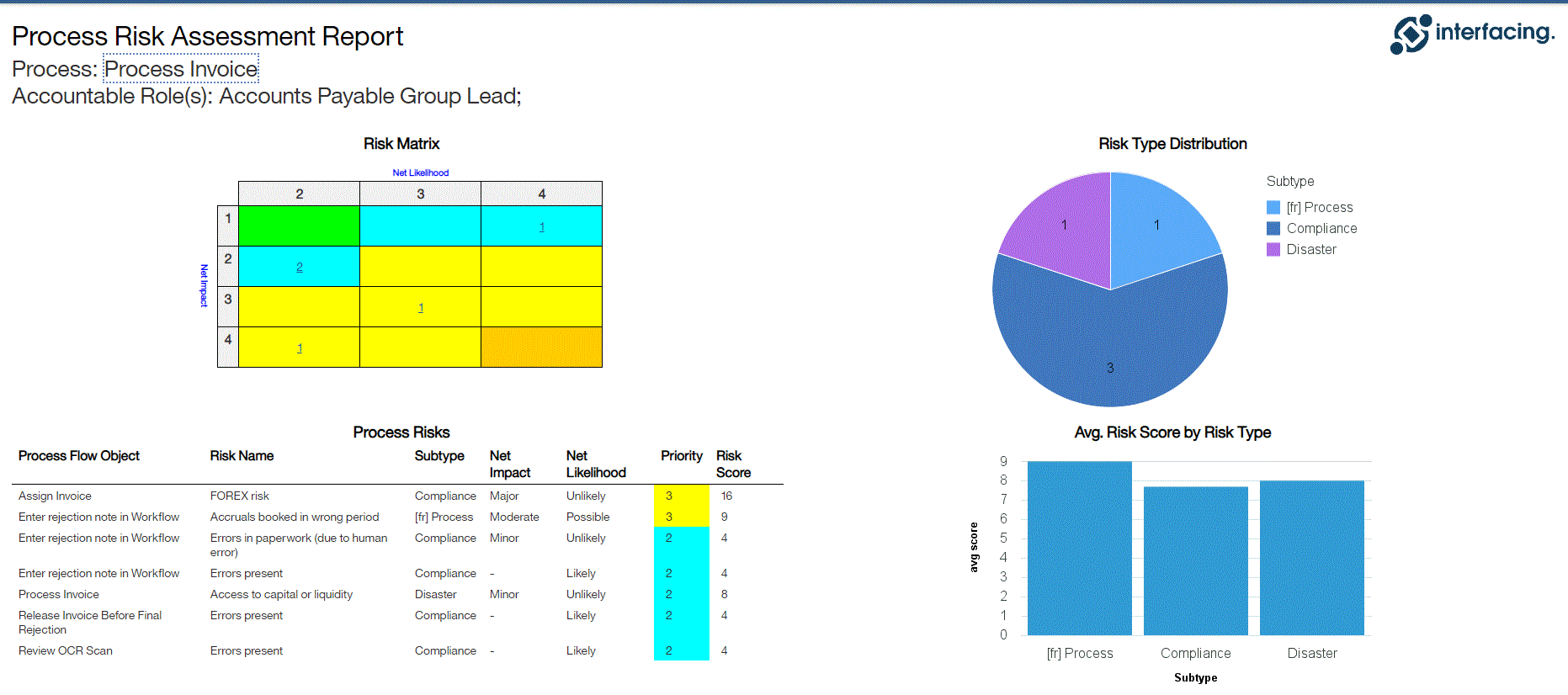
- Matrices de riesgo personalizables que incluyen probabilidad de riesgo, impacto, puntuación, porcentaje, color y prioridad
- Importación/exportación de datos de riesgo a través de Excel
- Visibilidad del proceso de principio a fin asociado a los riesgos
- Filtrar, buscar e informar de los riesgos por atributos
- Riesgos y controles reutilizables
- Activar las CAPA en función del análisis de riesgos de los procesos y las tareas
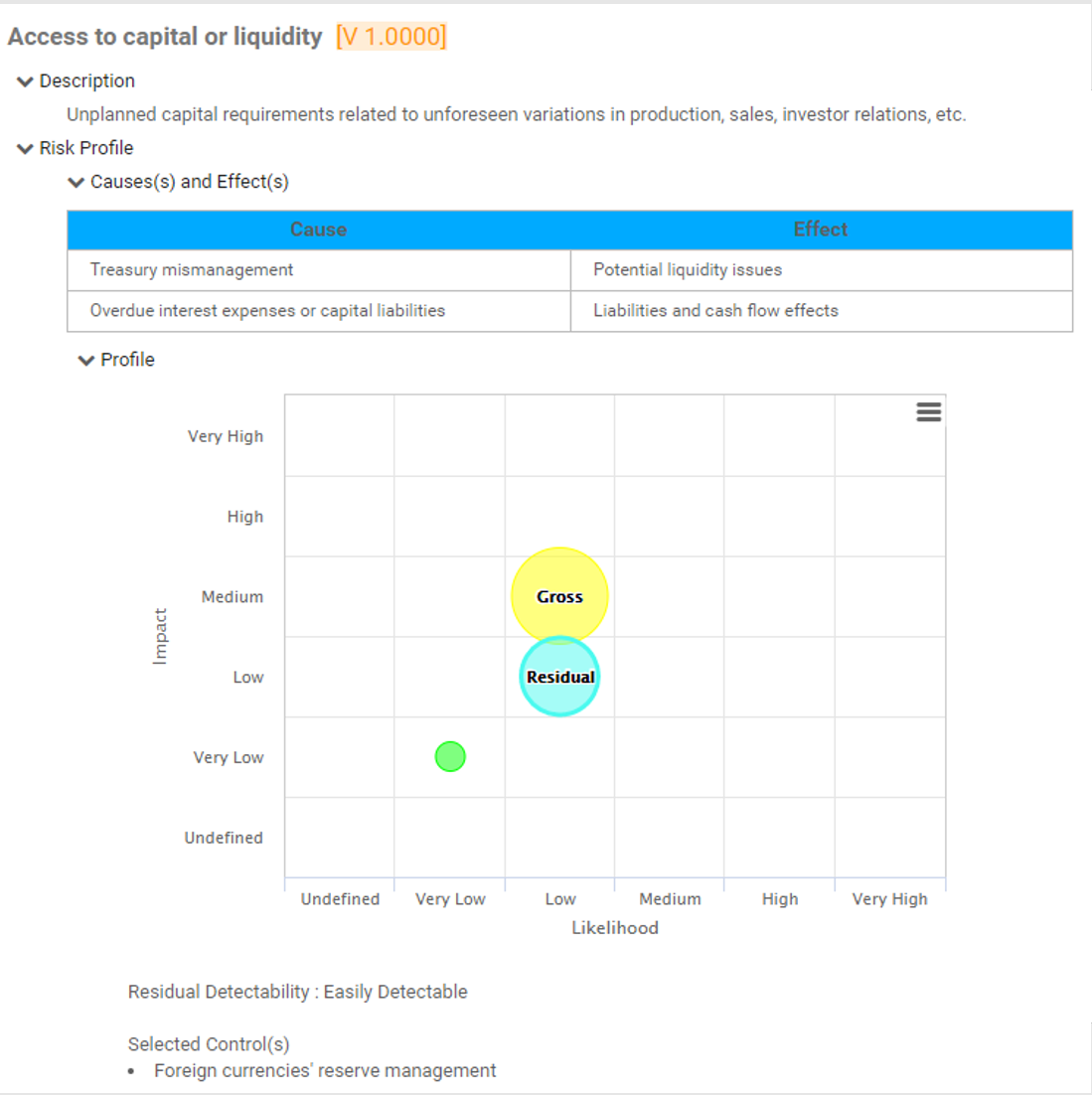
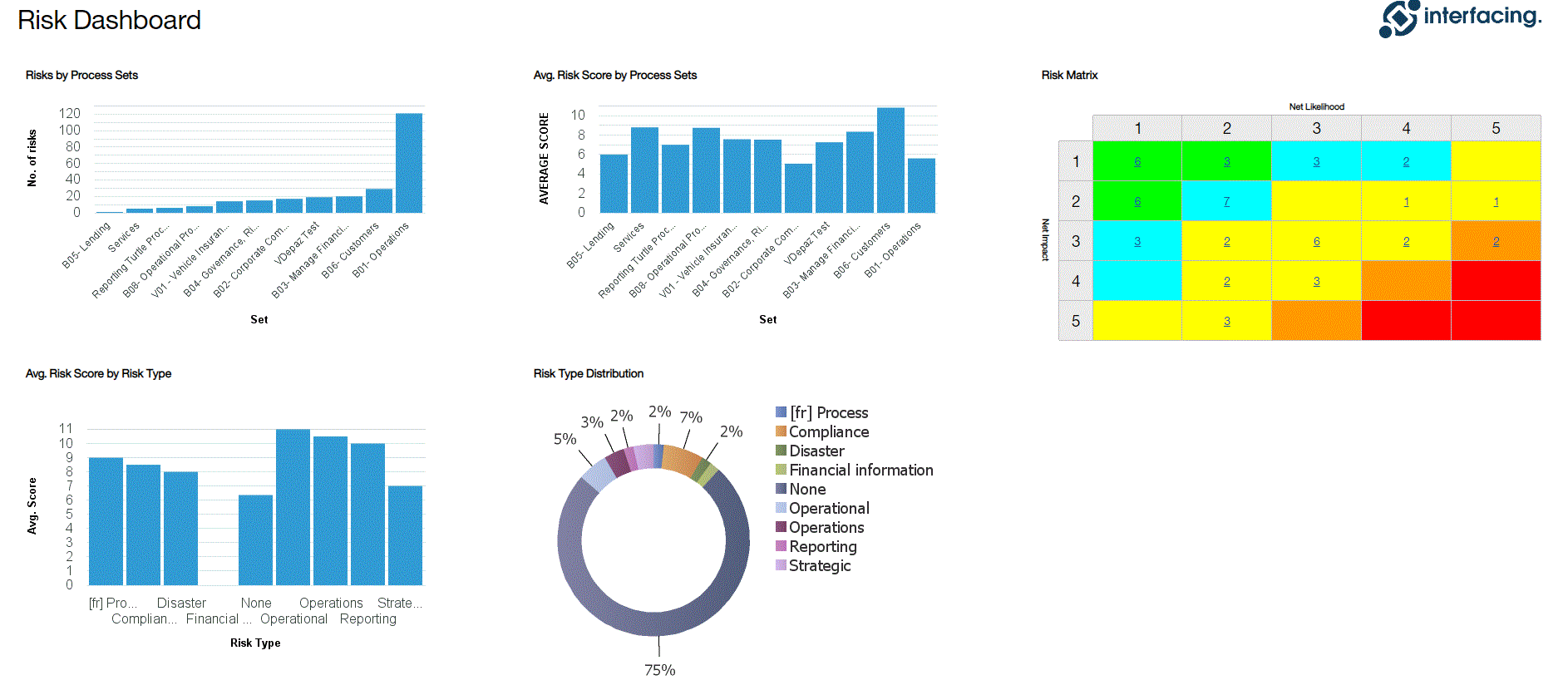
Ver la causa y el efecto de los riesgos para hacer un seguimiento de la información crítica sobre los riesgos; los gestores de riesgos analizan y priorizan la mitigación de los mismos
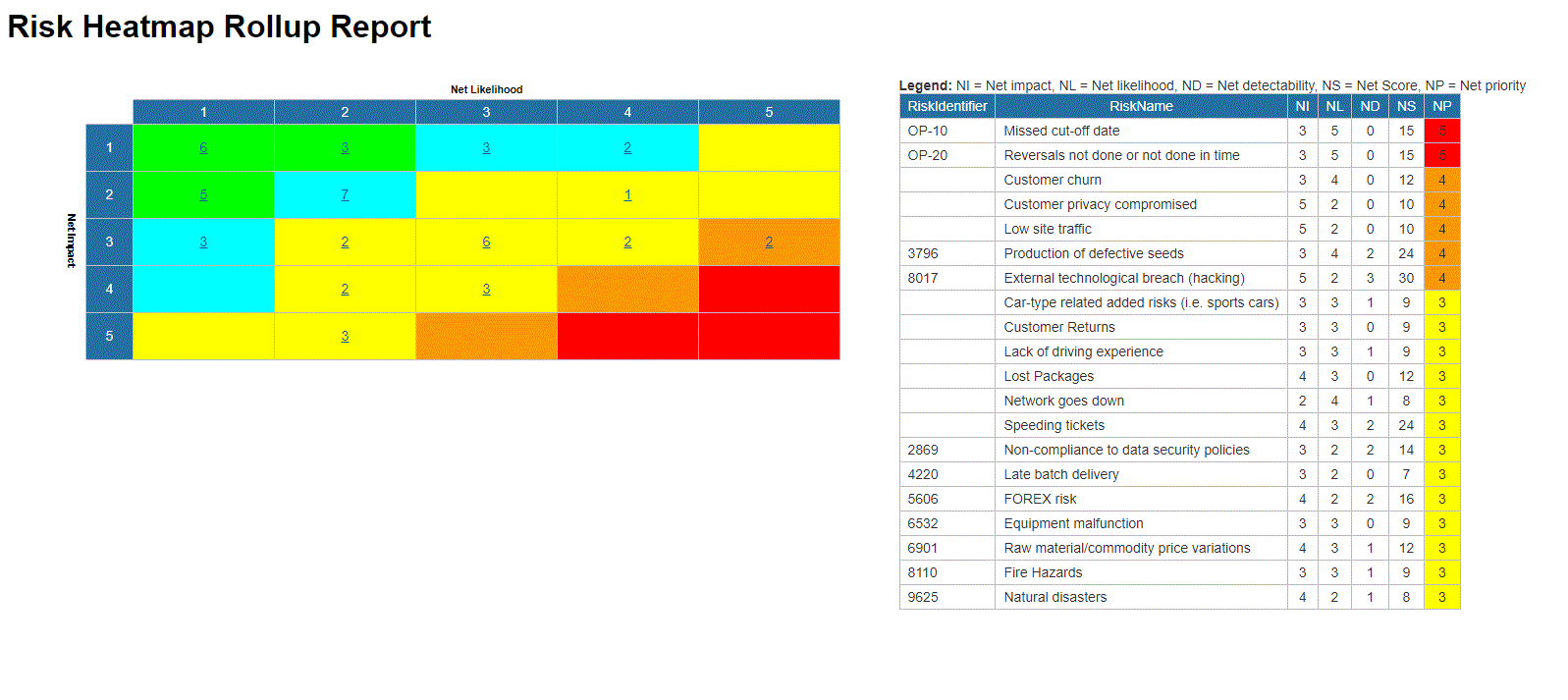
Edición de riesgos ampliada (riesgo bruto por proceso, riesgo neto por control en el proceso, controles específicos por proceso, cálculo de anulación por proceso)
Detectar la ocurrencia de un riesgo; algoritmo automatizado para la calificación del riesgo
El riesgo residual proporciona una visión realista del impacto potencial
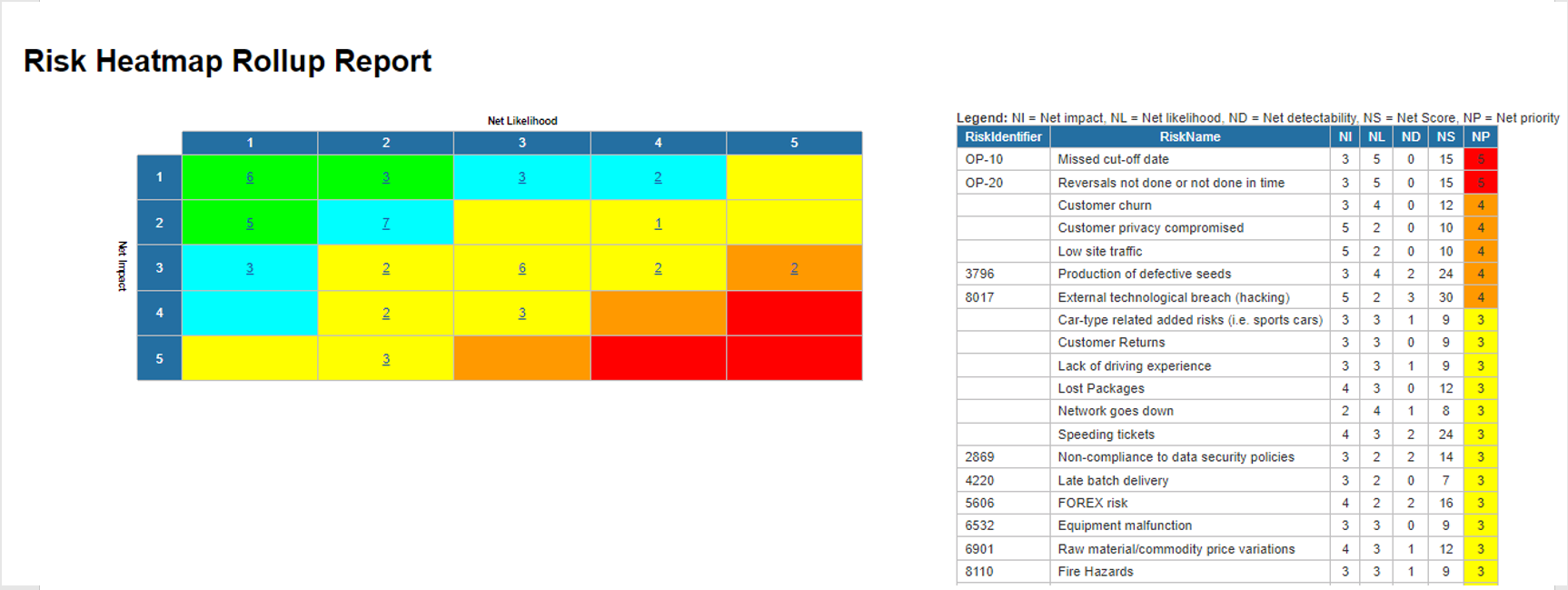
La matriz de riesgos visualiza 5 niveles diferentes de riesgos que residen en los procesos
Gestión de la capacitación
El reto actual en materia de formación es gestionar realmente la cantidad y la frecuencia de la formación que se imparte en todas las operaciones empresariales de la organización. Este reto es el que más afecta al seguimiento singular de un empleado concreto. La plataforma Digital Business de Interfacing apoya la gestión de la formación de su empresa gracias a su capacidad para enlazar sin esfuerzo con todos los sistemas de gestión del aprendizaje (LMS) de la organización.
Mida la eficacia de la formación a través de cuestionarios o pruebas controladas después de una sesión de formación completada para garantizar que su programa de gestión de la formación cumple con los requisitos reglamentarios y alcanza con éxito el alto umbral de conocimiento institucional de su organización.
Esto proporciona a los administradores de la capacitación visibilidad en todas las plataformas de capacitación relacionadas con los requisitos normativos, los procesos, los documentos y la propia capacitación. Piensa en ello como un depósito central para controlar y seguir toda la capacitación.
Características principales:
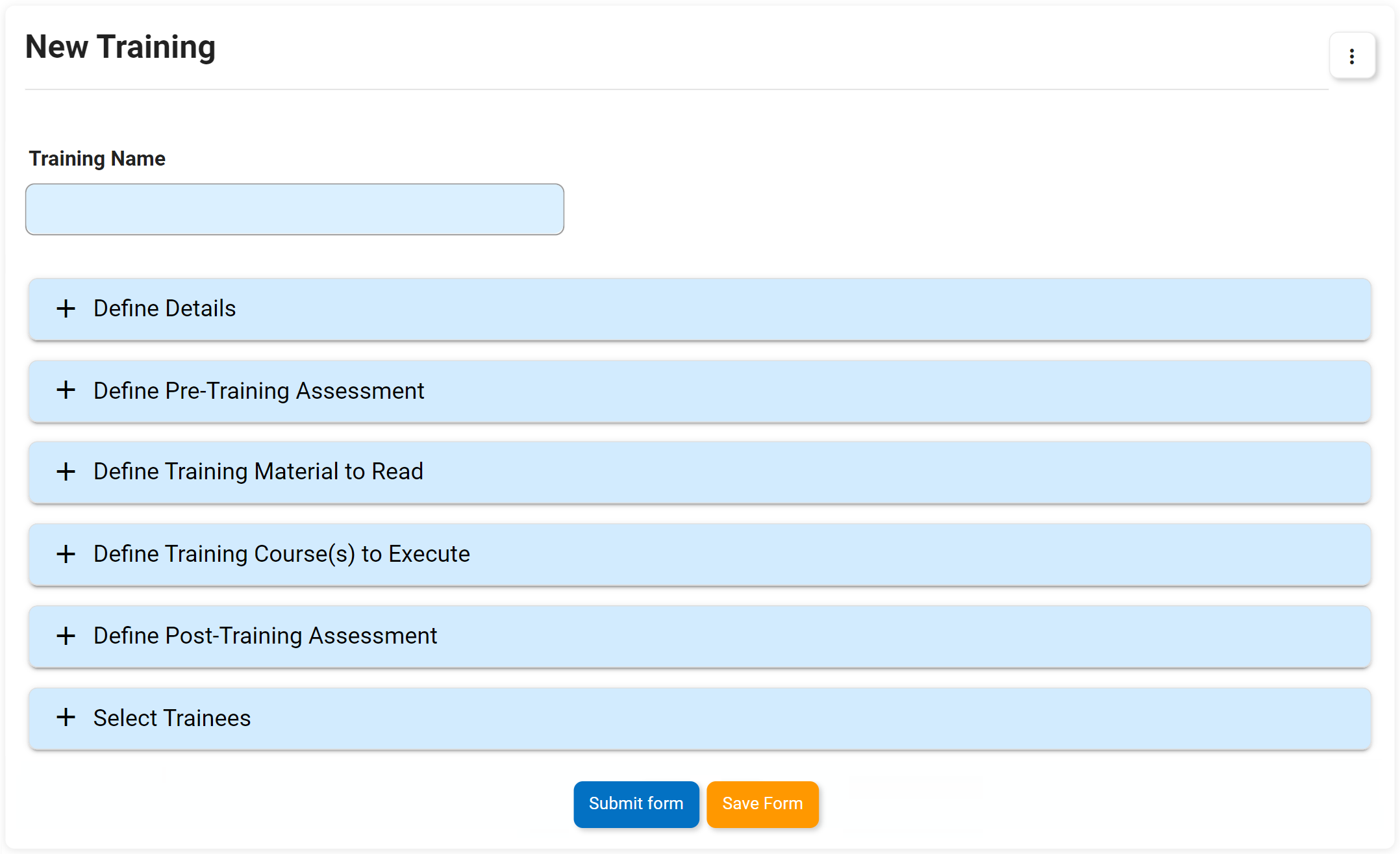
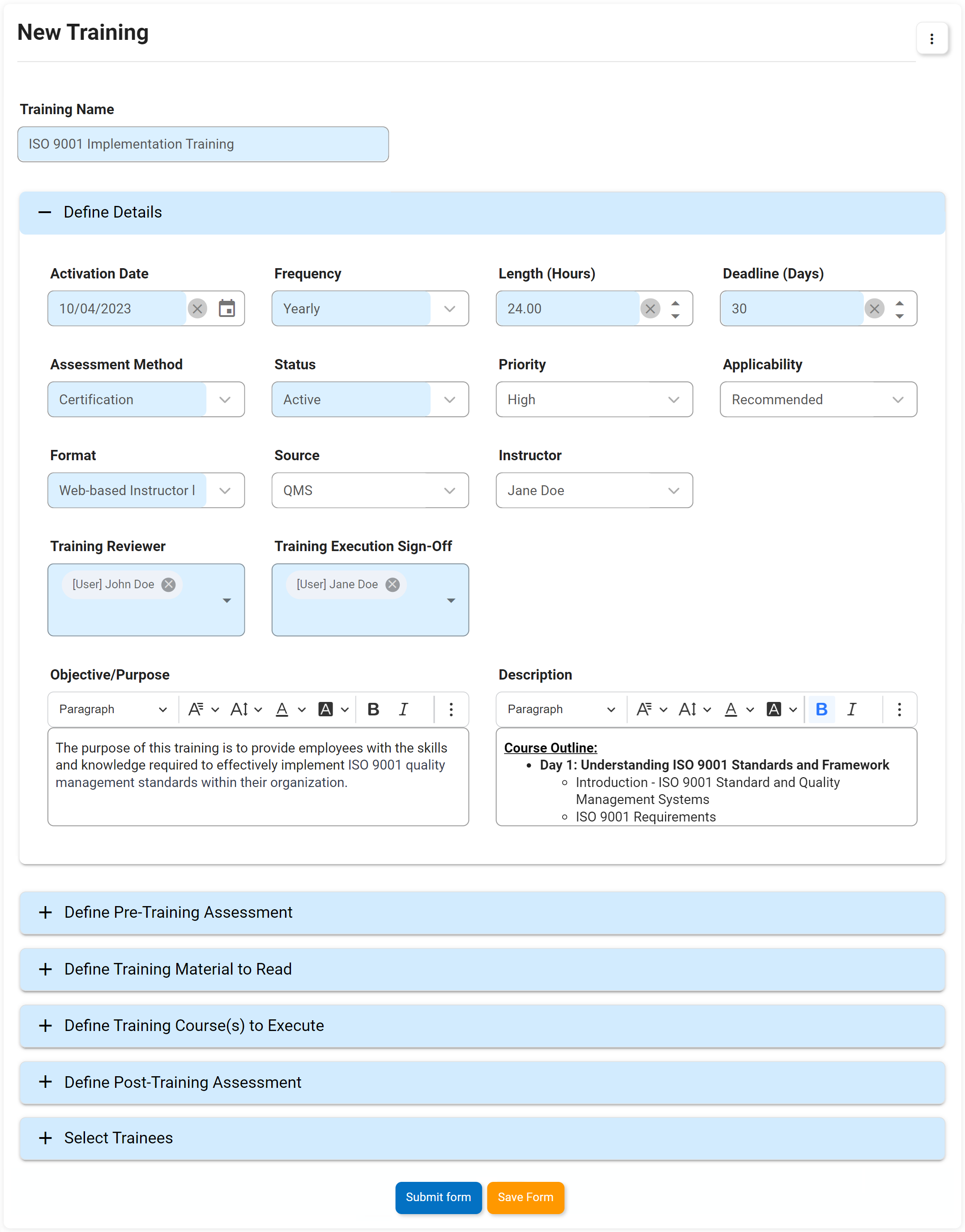
- Definir cuestionarios personalizados previo y posterior a la capacitación para medir la eficacia
- Aproveche los cuestionarios estándar para crear rápidamente nuevas plantillas de capacitación
- Proporcionar un enlace directo a los materiales de capacitación
- Reutilizar los requisitos de cumplimiento documentados en el repositorio IMS (normativa, documentos, procesos)
- Asignar la capacitación de forma dinámica
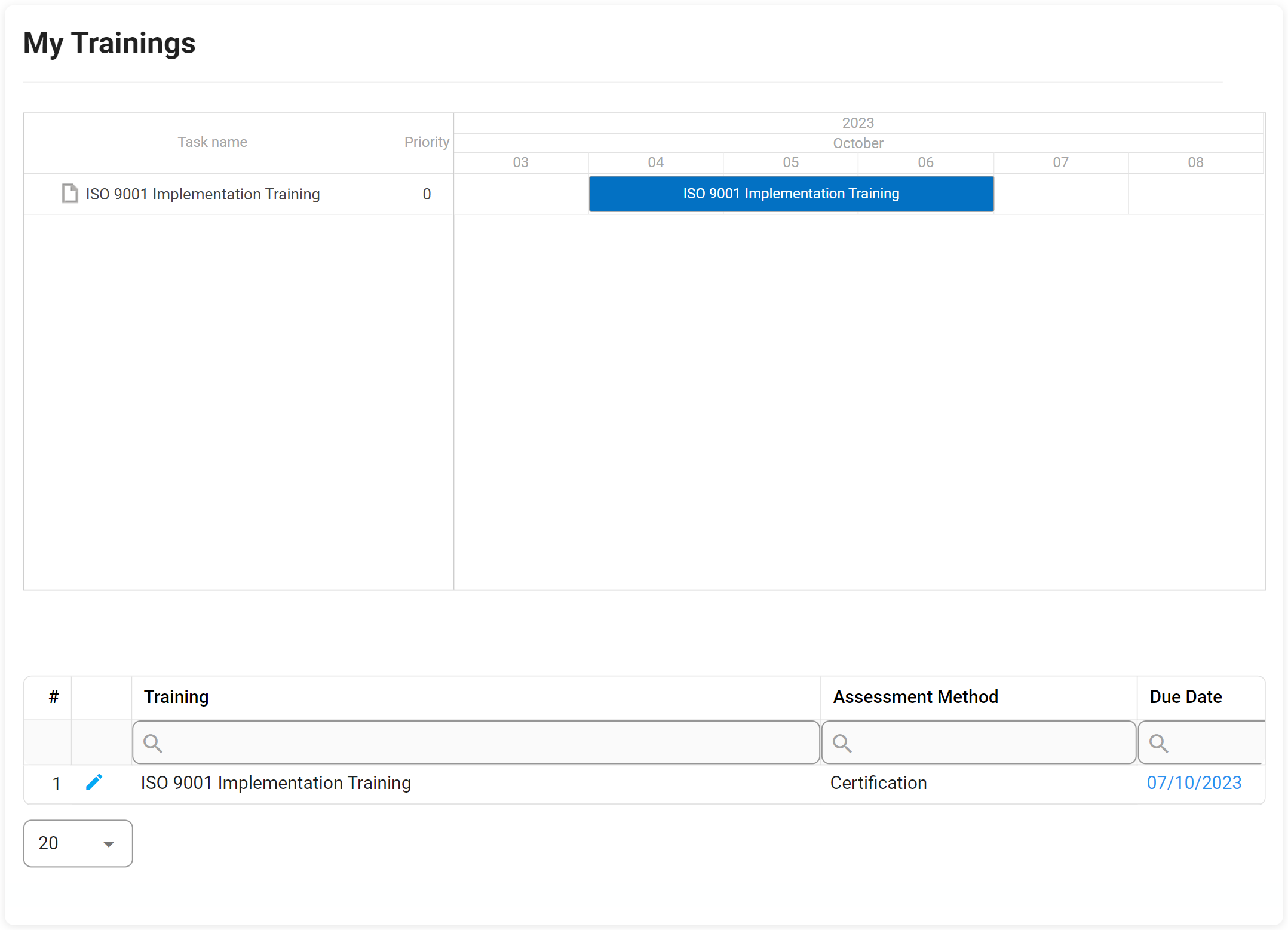
- Proporcionar a los usuarios una vista de calendario / Gantt de sus capacitaciones
- Proporcionar a los instructores una visión de sus cursos
- Desactivar el entrenamiento después del uso
- Solicitud de prórroga para la capacitación
- Los gestores deben dar el visto bueno a la capacitación tras su finalización
Gestión del control: Auditoría de indicadores de riesgo, análisis e informes,
EPC ofrece dentro de una única plataforma colaborativa un área donde los analistas pueden identificar, evaluar y priorizar los planes de mitigación de riesgos, y los auditores pueden programar y luego ejecutar auditorías de control e implementar planes de acción correctiva basados en los resultados de las pruebas. Además, mediante la identificación de indicadores clave de riesgo y control y la cuantificación de los límites de los umbrales, la administración puede supervisar las medidas para garantizar el cumplimiento de las políticas y el mantenimiento de las normas.
Características principales:
- Supervisar los controles mediante auditorías
- Programación de auditorías recurrentes
- Implementar CAPAs basadas en los resultados de las pruebas
- Cubo COSO Marco ERM
- Análisis general, análisis de rutas críticas y análisis de rutas de alto riesgo generados de forma dinámica
- Informe de controles y riesgos generales e informe personalizado
- Indicadores clave de riesgo y control (KRIs, KCIs) reutilizables para más de una fuente
- Fijación del umbral de objetivos para la mejora continua
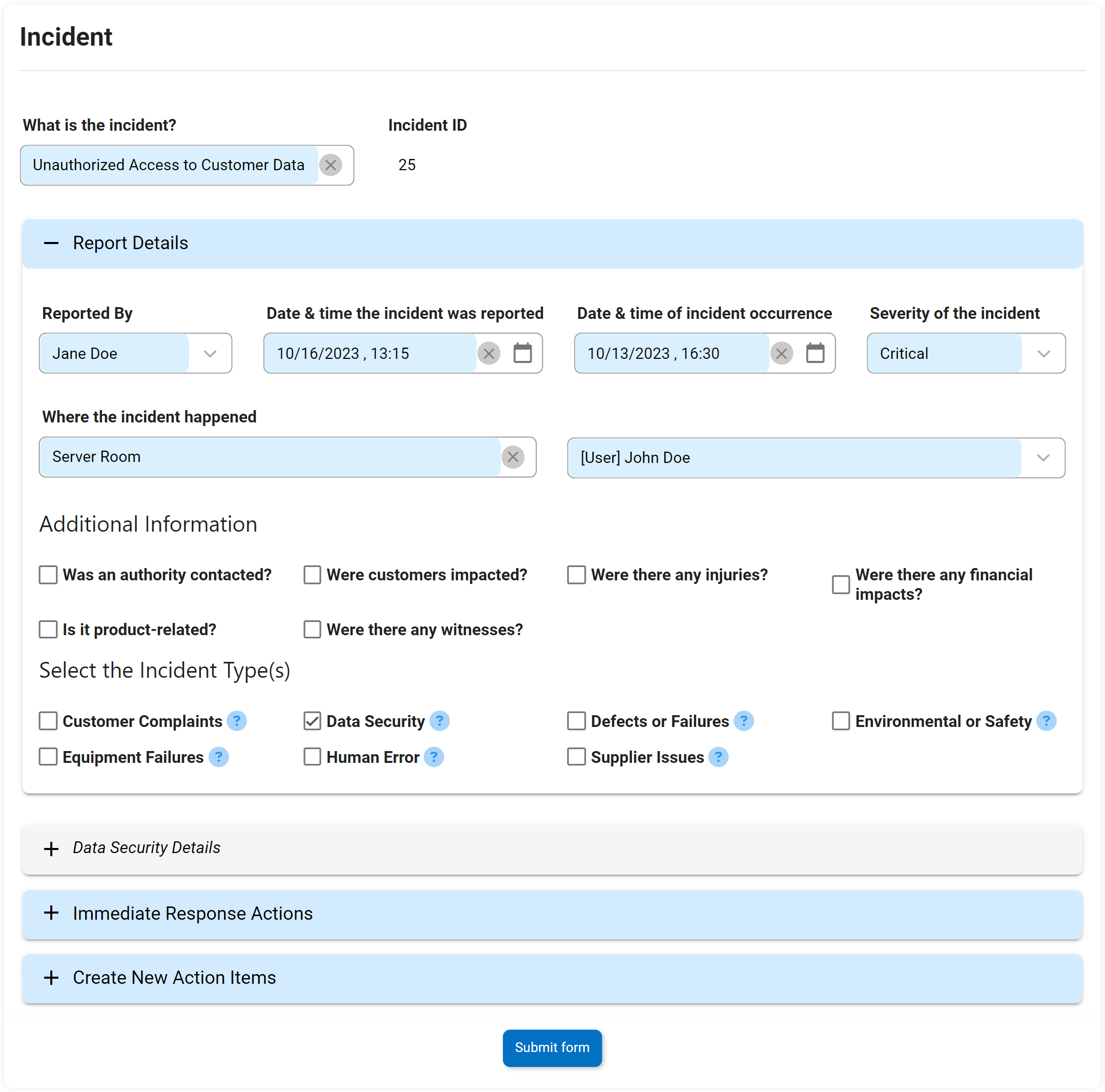
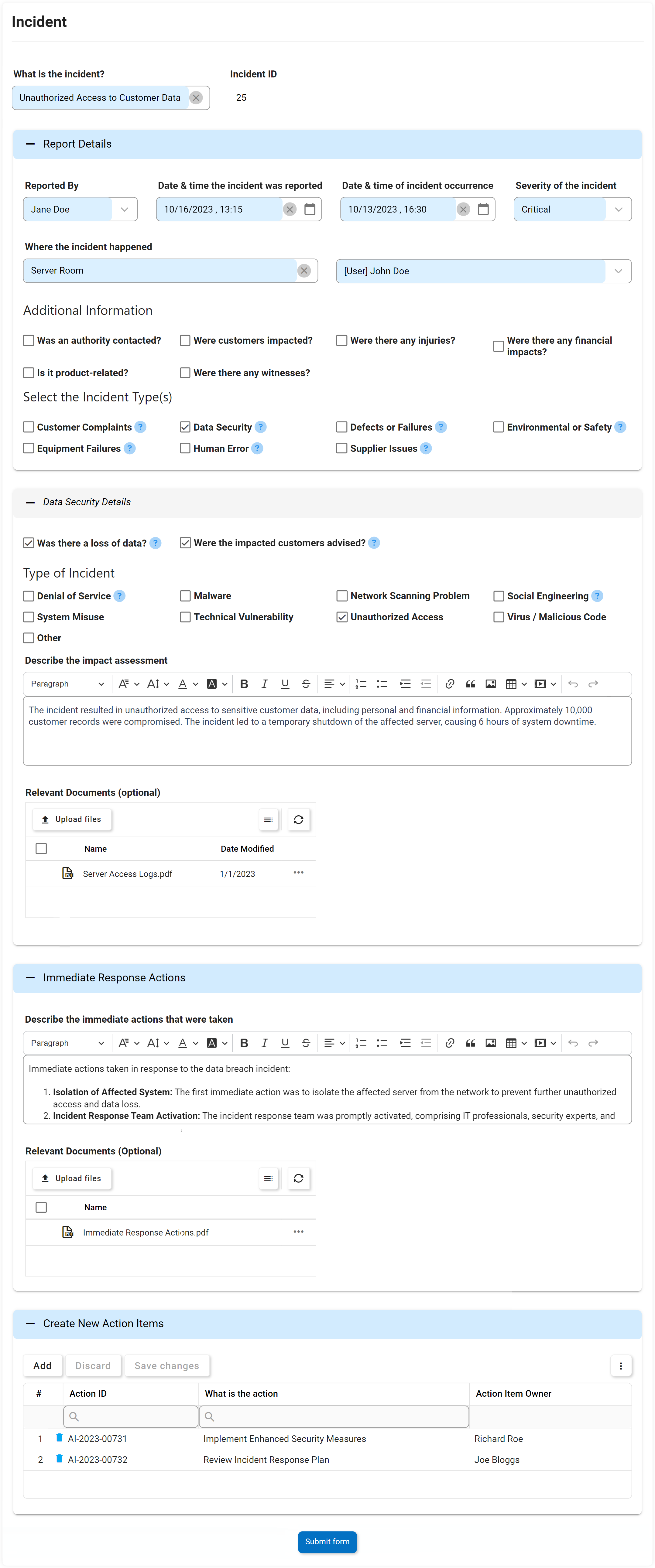
Administracion de incidentes
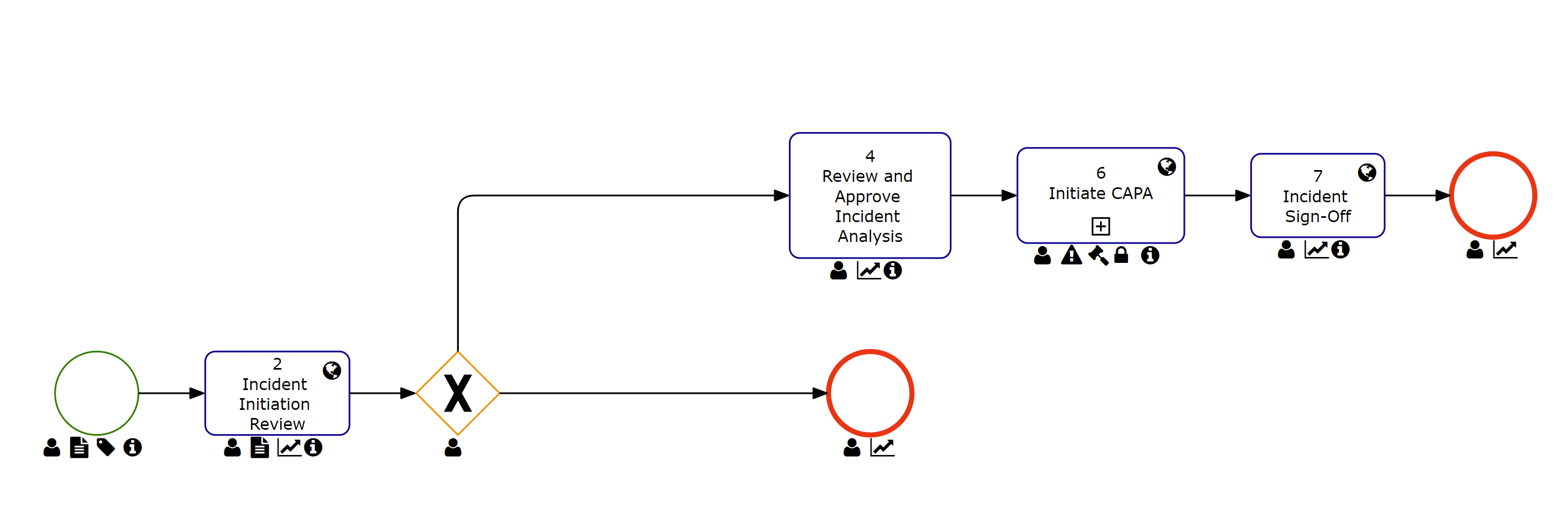
Los procedimientos y acciones que se toman para responder y resolver los incidentes que se producen se conocen como Gestión de Incidentes. El DBP de Interfacing apoyará estas acciones mediante el seguimiento y la escalada de la remediación de principio a fin. El DBP llevará a cabo un análisis de causa raíz (RCA) y un análisis de incidentes.
Una solución de plataforma empresarial digital garantiza que todas las incidencias se aborden con rapidez y se mantengan altos niveles de calidad. Los equipos también se benefician de las mejoras en las operaciones, evitando que se repitan futuros incidentes.
Características principales:
- Reutilizar la información de las etapas anteriores del proceso de un incidente
- Realización de análisis de causas y de riesgos
- Establezca múltiples ciclos de revisión y aprobación
- Activar una escalada a CAPA si es necesario
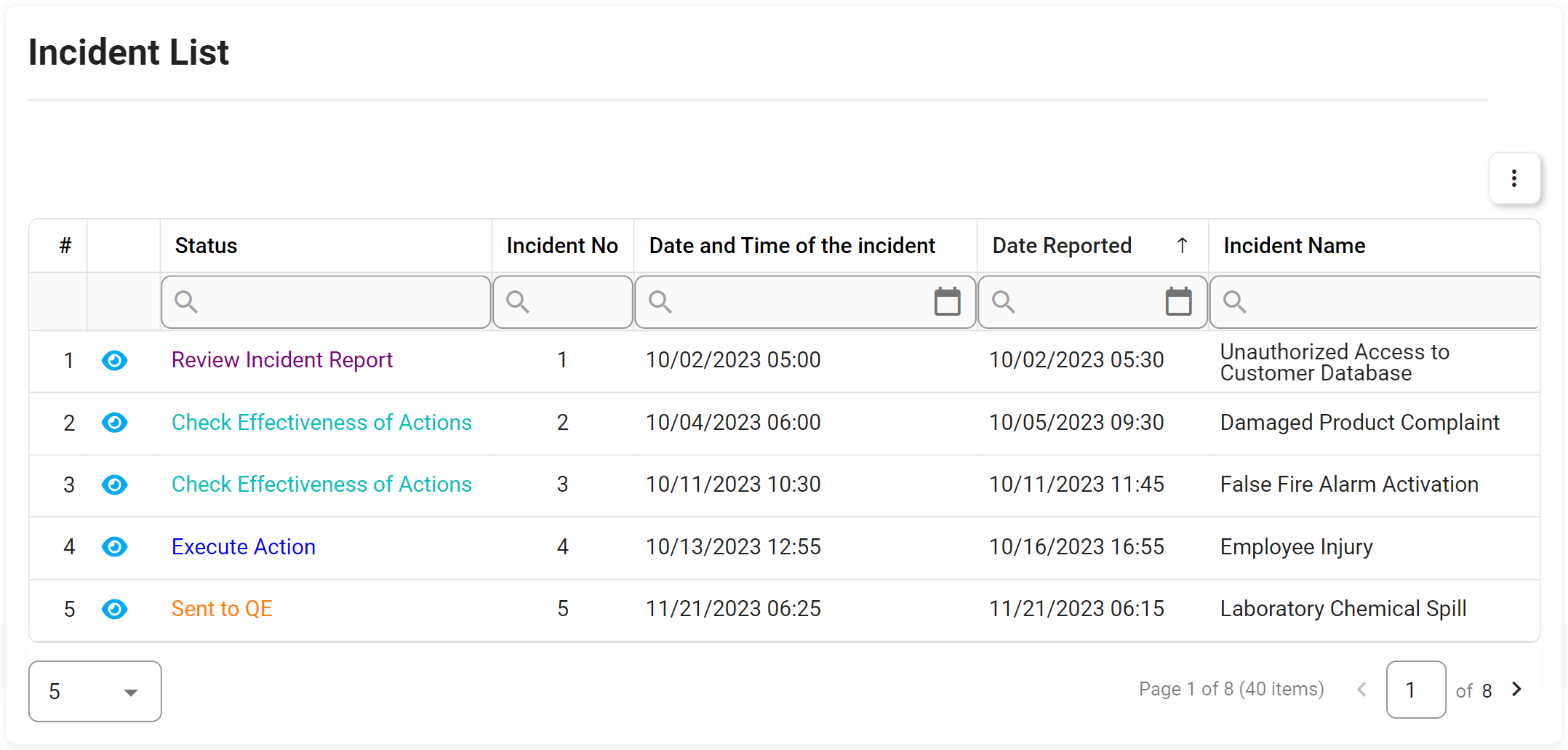
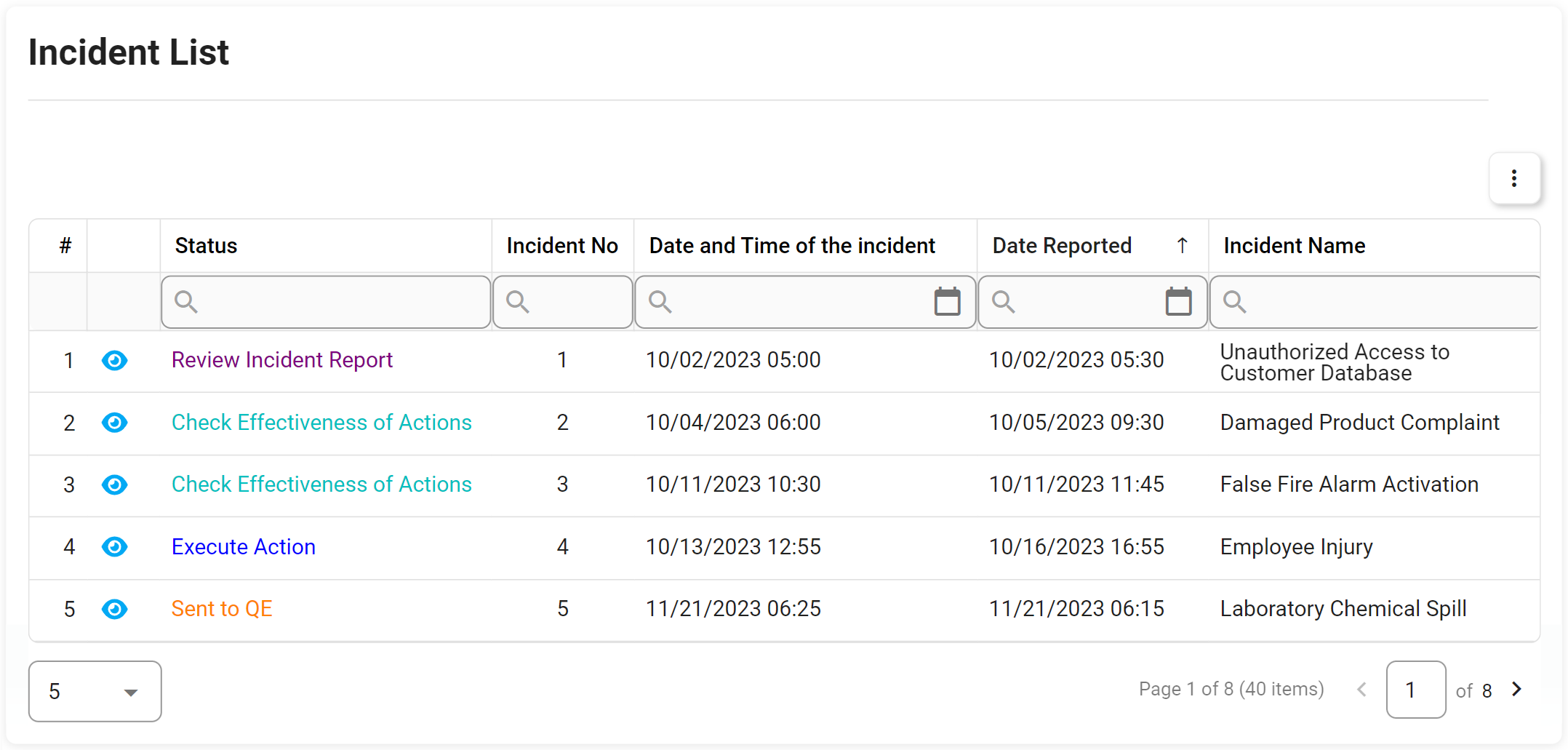
- Seguimiento del incidente con código de seguimiento en cualquier etapa del proceso
- Informes de incidentes con desgloses detallados para ver subconjuntos de información relativa
- Investigación de incidentes con confirmación de finalización mediante firma electrónica
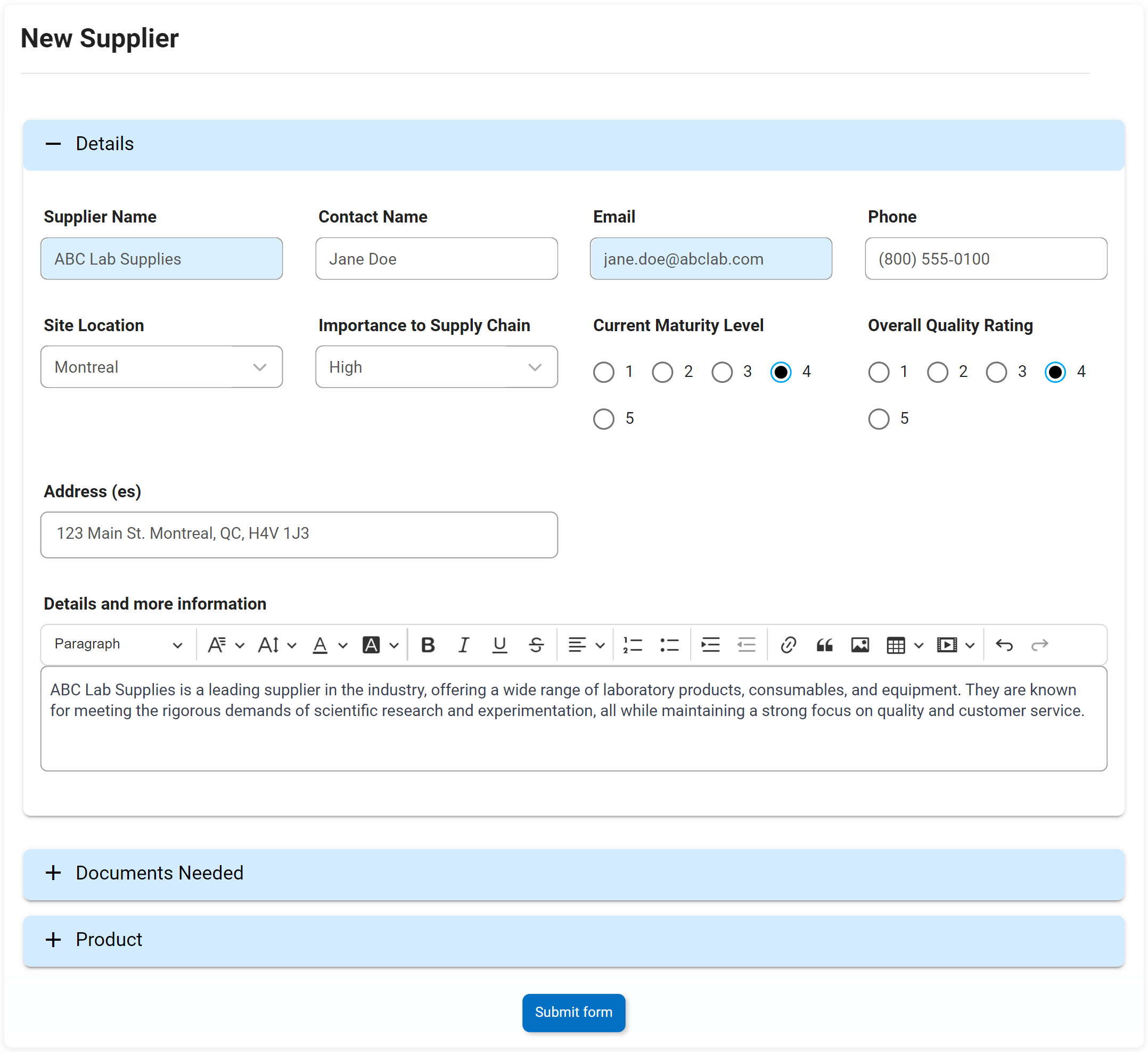
Gestión de proveedores y productos / SCAR
Características principales:
- Llevar a cabo un análisis de causa raíz (ACR)
- Aprovechar las mejores prácticas de metodologías de causa raíz(5 Ws, análisis comparativo, 3×5 Why)
- La causa raíz está integrada en el flujo de trabajo
- Enviar directamente las tareas a los usuarios como parte del flujo de trabajo del SCAR
- Plantear las acciones a los proveedores (SCAR)
- Reutilizar la información de los proveedores gestionada de forma centralizada
- Notificar directamente al proveedor
- Ver/editar/añadir múltiples elementos de acción del SCAR
- Funciones responsables y estado de los elementos de acción disponibles en tiempo real
eQMS y conformidad
Entendemos que los requisitos impuestos a las organizaciones en términos de cumplimiento son muy altos y que ISO9000, ISO13845, ISO17025, ISO27001, SOC 2, FDA QSR y GxP son una parte esencial de ese programa. Al utilizar nuestras soluciones, su empresa obtiene la responsabilidad y la coherencia que le brindarán una ventaja sobre la competencia. Nuestras herramientas garantizan una visibilidad completa de extremo a extremo, desde la creación y modificación de un reglamento hasta la aprobación y revisión del contenido hasta la actualización y readaptación de los empleados para los procedimientos operativos estándar (SOP). Vemos la administración completa del ciclo de vida como partes móviles de un ecosistema completo y es por eso que son un enfoque único que combina los requisitos reglamentarios, documentos, procesos, instrucciones de trabajo y gobernanza.
Estándar internacional que especifica los requisitos de un SGC. (Sistema de gestión de calidad con sus siglas en inglés eQMS) Es el estándar más popular de la serie ISO 9000 y el único estándar de la serie que las organizaciones pueden certificar.
Publicado por primera vez en 1987 por la Organización Internacional de Normalización (ISO). La versión actual de ISO 9001 se lanzó en septiembre de 2015.
En resumen, ISO 13485 es un estándar reconocido internacionalmente que han adoptado los siguientes países: Europa, Canadá, Australia y otros mercados. Excluyendo Canadá, la aplicación de ISO 13485 no es un requisito, pero es el estándar de facto que se usa hoy en día como una medida del cumplimiento total del SGC establecido en las regulaciones de dispositivos médicos.
La norma ISO/IEC 17025 define los requisitos generales de competencia en materia de ensayos y calibración para todos los laboratorios. Para los laboratorios de ensayo y calibración, ésta es la norma ISO definitiva.
En muchas ocasiones, las autoridades reguladoras y los proveedores no aceptan los resultados de las pruebas o de la calibración de un laboratorio que funciona independientemente de cualquier supervisión de la acreditación. Aquí es donde entra en juego la norma ISO/IEC 17025 (originalmente conocida como Guía 25 de ISO/ISO/IEC 17025).
La ISO 27000 es una serie de normas diseñadas para salvaguardar los activos de información de las organizaciones. La norma ISO 27000 también ofrece una visión general de un Sistema de Gestión de la Seguridad de la Información(SGSI), definiendo y describiendo el conjunto de procesos lógicamente organizados que guían a las organizaciones para alinear sus metas y objetivos empresariales con su seguridad de la información.
Menos conocida que la versión más larga, "Controles de Sistemas y Organizaciones 2", SOC 2 (o SOC II) es un marco utilizado para ayudar a las empresas a demostrar los controles de seguridad que existen para proteger los datos de los clientes en la nube. Estos controles pasaron a conocerse como Servicios de Confianza Principios: Seguridad, Disponibilidad, Integridad del Proceso, Confidencialidad y, por último Privacidad.
Otros países tendrán sus propios criterios para cumplir con los requisitos específicos del SGC. Por ejemplo, si bien Brasil y Japón tienen sus propios requisitos, ambos se basan en las normas QSR e ISO 13485 de la FDA de EE. UU. Existentes.
En una nota positiva, estos estándares logran requisitos de gestión de calidad armonizados para cumplir con los estándares de QMS de EE. UU., Canadá, Europa y todos los demás vigentes.
La QSR de la FDA de EE. UU. (También conocida como 21 CFR Parte 820) se introdujo antes de la norma ISO 13485. Todas las empresas de dispositivos médicos en los EE. UU. Deben cumplir con este estándar para la distribución nacional, pero deben cumplir con ambas regulaciones para distribuir dispositivos a nivel internacional. Las QSR de la FDA de EE. UU. También deben ser satisfechas por las empresas internacionales que deseen hacer negocios con clientes de EE. UU.
Como parte de nuestro compromiso continuo con el cumplimiento y la garantía de que nuestros clientes cumplan con sus requisitos regulatorios, siempre estamos en la búsqueda de maneras de ayudar a nuestros clientes a alcanzar y mantener el pleno cumplimiento. Interfacing cuenta con la certificación ISO 27001 y nos asociamos con Amazon Web Services (AWS) para el alojamiento en la nube, ya que se ha demostrado su compromiso con el cumplimiento, con el cumplimiento global de los centros de datos con SOC 1 Tipo II e ISO 27001. Para obtener más información sobre el cumplimiento de AWS para ISO 18345, FDA QSR y GxP, consulte su Programa de cumplimiento .
¿Por qué Interfacing?
Elimine la carga de cumplimiento y mejore la calidad del producto mediante la automatización de procesos de calidad críticos como documentos, eventos de calidad, capacitación, cadena de valor y gestión de auditorías en una única solución EQMS de Enterprise Process Center de extremo a extremo.
Para obtener más información o hablar sobre cómo Interfacing puede ayudar a su organización, rellene el siguiente formulario.
Ciencias Biológicas y Farmacéutica
Al adoptar una cultura sólida y centrada en los procesos, su empresa puede pasar sin problemas de sistemas de gestión caóticos y ad hoc a un funcionamiento fluido. cumple con las normativas operación.
QMS de tecnología de dispositivos médicos
Todos los aspectos del proceso de tecnología médica deben ser controlados y monitoreados según los requisitos de la norma ISO 13845 y QSR de la FDA de EE. UU. Lee mas aquí .
Obtenga transparencia con Enterprise Process Center®
El software Digital Twin Organization de Interfacing proporciona la transparencia y la gobernanza para mejorar la calidad, la eficiencia y garantizar el cumplimiento normativo.
Lea nuestros blogs
¡Tómese un momento para leer blogs sobre GXP, cumplimiento normativo, tendencias actuales y mucho más!
Descubra cómo su organización se beneficia de una solución centrada en Interfacing eQMS.
Un diferenciador clave de Interfacing con otras firmas de consultoría de transformación digital y empresarial es que Interfacing ofrece su propia solución tecnológica innovadora en apoyo de los programas de transformación.
Las soluciones compatibles con eQMS ofrecen la transparencia necesaria para reducir la complejidad, mejorar la ejecución y facilitar la agilidad y el cambio.
La solución de sistema de gestión integrada eQMS de Interfacing es una ventanilla única para gestionar programas de transformación. Sabemos que existe un entorno muy competitivo. Es por esa razón que nuestra fortaleza está en nuestro compromiso de mantener la flexibilidad durante todo el ciclo de vida del proyecto, ya sea en nuestros productos innovadores o en nuestro equipo de expertos.